题目内容
【题目】“对比实验”是化学学习中行之有效的思维方法.某化学学习小组的同学走进实验室做了如下实验,请你参与并回答下列问题: 
(1)通过实验A,观察到乒乓球片先燃烧,可以说明燃烧的条件之一是 , 实验中使用铜片,是利用了铜的性.
(2)对于实验B,一段时间后观察到试管①中的铁钉明显锈蚀,由此得出:铁生锈的主要条件是铁与和直接接触.铁锈疏松多孔,需要及时除去,除去铁制品表面的铁锈可用 , 反应的化学方程式是 , 属于反应(填反应类型).
(3)通过实验C,可得出的结论是(填字母).
A、①②B、②③C、③④D、①④
①CO2密度比空气大 ②CO2不支持燃烧
③CO2不能使干石蕊纸花变色 ④CO2能够与水发生化学反应,反应的化学方程式是 .
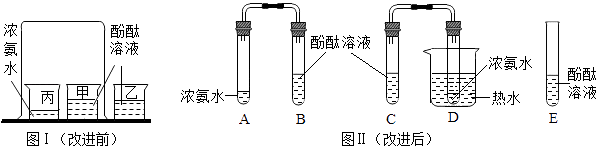
(4)实验D的烧杯②中呈现的现象能说明分子是不断运动的.
当烧杯①中液体是浓氨水时,烧杯②中的酚酞溶液由无色变为色;
当烧杯①中液体是浓盐酸,烧杯②中液体是滴有两滴氢氧化钠的酚酞溶液时,一段时间后,溶液颜色的变化是 , 写出该反应的化学方程式 .
【答案】
(1)温度需达到可燃物的着火点;导热
(2)空气;水;盐酸;6HCl+Fe2O3═2FeCl3+3H2O;复分解
(3)C;CO2+H2O=H2CO3
(4)红;红色逐渐褪去变为无色;HCl+NaOH═NaCl+H2O
【解析】解:(1)燃烧的条件:物质具有可燃性、与氧气接触、温度达到可燃物的着火点,实验A中滤纸碎片和乒乓球碎片都与氧气接触,在加热过程中,利用铜片的导热性,在中间加热,能够提供均匀的热量,由于乒乓球碎片的着火点较低,首先燃烧起来,说明燃烧需要温度达到可燃物的着火点;
故填:温度需达到可燃物的着火点;导热;(2)对于实验B,一段时间观察试管①中的铁钉明显锈蚀,①试管中即提供了空气,也提供了水,由此得出:铁生锈的主要条件是铁与水和空气直接接触;铁锈的主要成分是氧化铁,所以欲除去铁锈可用盐酸洗方法,氧化铁与稀盐酸反应生成氯化铁和水,该反应是由两种化合物相互交换成分生成两种新的化合物,属于复分解反应;故填:空气;水;盐酸;6HCl+Fe2O3═2FeCl3+3H2O;复分解;(3)二氧化碳不能使纸花变色,而二氧化碳与水反应生成碳酸,碳酸使纸花变成了红色;不能说明二氧化碳的密度比空气大,也不能证明二氧化碳不支持燃烧;故填:C;CO2+H2O=H2CO3;(4)实验D的烧杯②中呈现的现象能说明分子是不断运动的.当烧杯①中液体时浓氨水时,浓氨水具有挥发性,挥发出的氨气溶于水显碱性,所以烧杯②中的酚酞溶液由无色变为红色;当烧杯①中液体换成浓盐酸,浓盐酸具有挥发性,挥发出的氯化氢气体溶于水显酸性,烧杯②中液体换成滴有酚酞NaOH溶液时,一段时间后,溶液颜色的变化是红色逐渐褪去变为无色.其中盐酸与NaOH反应生成氯化钠和水,反应的化学方程式为HCl+NaOH═NaCl+H2O.
所以答案是:红;红色逐渐褪去变为无色;HCl+NaOH═NaCl+H2O.
【考点精析】根据题目的已知条件,利用二氧化碳的化学性质和金属的物理性质及用途的相关知识可以得到问题的答案,需要掌握化学性质:一般情况下不能燃烧,也不支持燃烧,不能供给呼吸;与水反应生成碳酸;能使澄清的石灰水变浑浊;与灼热的碳反应;金属的物理性质: (1)常温下一般为固态(汞为液态),有金属光泽.(2)大多数呈银白色(铜为紫红色,金为黄色)(3)有良好的导热性、导电性、延展性.

 全能测控期末小状元系列答案
全能测控期末小状元系列答案