题目内容
【题目】a、b、c 三种物质的溶解度曲线如下图图 2 所示,据题意回答下列问题:
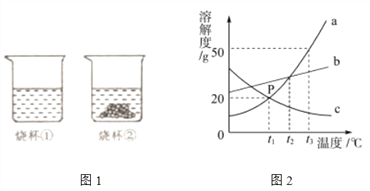
(1)图 2 中 P 点的含义是______________________________________________。
(2) 要使接近饱和的 c 物质溶液变为饱和,可采取的一种措施是______________________________。
(3)t3℃时,将等质量的 a、b、c 三种物质的饱和溶液同时降温至t1℃时,析出晶体最多的是_____,所得溶液中溶质质量分数由小到大的顺序是______。
(4) a 固体中有少量 b,现有提纯 a 物质涉及到的操作步骤:①溶解、②过滤、③______(填“降温结晶”或“蒸发结晶”)、④加热浓缩。则提纯的它的步骤顺序是_______________(填操作序号)。
(5)t1℃时,现将等质量的 a 和 b 分别加入到各盛有 100g 水的两个烧杯中,充分搅拌后现象如图 1 所示。如果把图 1 所示的两个烧杯升温至t2℃,试判断t2℃时烧杯②中溶液一 定是__(填“饱和溶液”、“不饱和溶液”或“不确定”),且此时两烧杯中溶质的质量分数大小比较是:烧杯①_______________烧杯②(填“大于”、“小于”或“等于”)。
【答案】 t1℃时,a、c 的溶解度相同为 20g 加 c 物质至不再溶解;恒温蒸发溶剂至有晶体析出;升温至有晶体析出 a c<a<b 降温结晶 ①④③② 不饱和溶液 等于
【解析】(1)由图可知,P点是a、c两物质溶解度曲线的交点,所以P 点表示t1℃时,a、c 的溶解度相同为 20g;
(2)c物质的溶解度随温度的升高而减小,要使接近饱和的 c 物质溶液变为饱和,可加 c 物质至不再溶解或恒温蒸发溶剂至有晶体析出或升温至有晶体析出;
(3)在t3℃时,将等质量的a、b、c三种物质的饱和溶液同时降温至t1℃时,a的溶解度变化最大,所以析出晶体最多;饱和溶液中溶质的质量分数=![]() ×100%,即溶解度大则溶质的质量分数大,降温过程中,ab溶解度减小,析出晶体,溶质的质量分数减小,c溶解度变大,溶液中溶质、溶剂的质量不变,所以溶质的质量分数不变,与降温前相等,t1℃时b的溶解度大于a的溶解度大于t3℃时c的溶解度,故所得溶液中溶质质量分数由小到大的顺序是c<a<b;
×100%,即溶解度大则溶质的质量分数大,降温过程中,ab溶解度减小,析出晶体,溶质的质量分数减小,c溶解度变大,溶液中溶质、溶剂的质量不变,所以溶质的质量分数不变,与降温前相等,t1℃时b的溶解度大于a的溶解度大于t3℃时c的溶解度,故所得溶液中溶质质量分数由小到大的顺序是c<a<b;
(4)a物质的溶解度随温度的升高而增大,b物质的溶解度随温度的升高影响不大,a 固体中有少量 b,提纯 a 物质,可用降温结晶的方法;所以提纯的它的步骤顺序是①溶解、④加热浓缩、③降温结晶、②过滤;
(5)t1℃时b的溶解度大于a的溶解度,烧杯①中是b,烧杯②中是b,由于烧杯①完全溶解,t2℃时,烧杯①②中物质的溶解度大于t1℃时烧杯①物质的溶解度,所以溶液升温到t2℃时,烧杯②中的物质全部溶解,并且都变为不饱和溶液;由于两个烧杯中物质质量相同且完全溶解,水的质量也相同,所以此时两烧杯中溶质的质量分数相等。

 阅读快车系列答案
阅读快车系列答案