题目内容
【题目】用化学用语填空:
(1)5个硫酸根离子_____
(2)表示氮气中氮元素的化合价_____
(3)最轻的且具有可燃性的气体是_____
(4)相对分子质量最小的氧化物是_____
(5)保持二氧化碳化学性质的最小粒子是_____
(6)地壳中含量最多的非金属元素与含量最多的金属元素组成的化合物的化学式是_____
【答案】5SO4 2﹣ ![]() H2 H2O CO2 Al2O3
H2 H2O CO2 Al2O3
【解析】
(1)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。表示多个该离子,在其离子符号前加上相应的数字,1个硫酸根离子带1个单位的正电荷,故5个硫酸根离子可表示为:5SO42﹣;
(2)氮气中氮元素的化合价为0价;由化合价的表示方法,在该元素的上方用正负号和数字表示,正负号在前,数字在后。表示氮气中氮元素的化合价可表示为2![]() ;
;
(3)氢气是最轻的且具有可燃性的气体,其化学式为:H2;
(4)相对分子质量为构成分子的各原子的相对原子质量之和;氧化物是只含有两种元素且其中一种元素是氧元素的化合物,相对分子质量最小的氧化物是水,其化学式为:H2O;
(5)二氧化碳是由二氧化碳分子构成的,保持二氧化碳化学性质的最小微粒是二氧化碳分子,其分子符号为:CO2;
(6)地壳中含量最多的金属元素是铝元素,含量最多的非金属元素是氧元素,组成的化合物为氧化铝,氧化铝中铝元素显+3价,氧元素显﹣2价,其化学式为:Al2O3。

【题目】某课外小组的同学利用老师提供的下列仪器、药品进行实验探究

(1)甲同学设计了两种制取氧气的方案
A 把二氧化锰加入盛有过氧化氢溶液的试管中;
B 把过氧化氢溶液缓缓加入盛有少量二氧化锰的试管中。
能得到平稳氧气流的是_____,(填A或B)
(2)老师提供的红砖粉末有什么作用?乙同学联想二氧化锰作过氧化氢的催化剂,于是想到红砖粉末是否也可以作过氧化氢的催化剂?请你一起参与探究,并回答有关问题
(猜想与假设)红砖粉末能作过氧化氢分解的催化剂。
(实验验证)乙同学设计了如下三个实验:
实验:取一定量过氧化氢溶液于试管中,观察到有极少量气泡产生,将带火星的木条伸入试管中,木条没有复燃。说明过氧化氢在常温下分解缓慢。
实验二:在实验一的试管中加入1克红砖粉末,有大量气泡产生,伸入带火星的木条,木条复燃。说明_____。
实验三:待反应结束后,将试管中的不溶物滤出,并洗涤、于燥、称量,固体的质量仍为1克,说明_____
(实验结论)乙同学认为红砖粉末可以作过氧化氢分解的催化剂。
(反思评价)丙同学认为要证明乙同学的结论正确,还需要再补充一个探究实验这一探究实验的目的是_____。
(拓展)下表是丁同学探究影响过氧化氢分解速率的因素时所记录的数据,通过对数据的分析,你得到的结论是_____。
催化剂及其质量 反应结束所需要的时间/min 过氧化氢溶液的浓度 | 30% | 15% | 5% |
W克二氧化锰 | 0.3 | 0.9 | 2.1 |
W克红砖粉末 | 8.0 | 10.0 | 17.0 |
【题目】某校化学兴趣小组的同学在老师的指导下做了有关氧气探究实验:
学习了二氧化锰对过氧化氢分解有催化作用的知识后,某同学想:CuO(氧化铜)能否起类似二氧化锰的催化作用呢?于是进行了以下探究。
(猜想与假设)
Ⅰ.CuO不是过氧化氢分解反应的催化剂
Ⅱ.CuO是过氧化氢分解反应的催化剂。
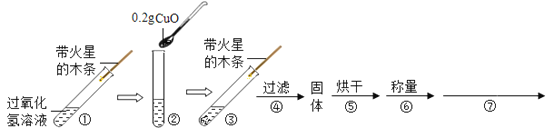
(实验探究)用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:
(1)
步骤③现象 | 步骤⑥结果 | 步骤⑦ | 结论 |
_____ | _____ | _____ | 猜想I不成立; 猜想Ⅱ成立。 |
(2)能证明CuO加快了过氧化氢分解速率的实验步骤是_____;
(3)证明CuO是过氧化氢分解的催化剂,需通过步骤⑦说明_____;
(4)小组同学通过互联网得知,CuSO4溶液也能显著加快过氧化氢的分解,CuSO4溶液主要含有三种粒子(H2O、Cu2+、SO42-),稀硫酸中含有三种粒子(H2O、H+、SO42-),为了进一步探究CuSO4,溶液中哪种粒子能起催化作用,小组同学作了以下分析和设计。
①小组同学认为最不可能的是H2O,他们的理由是_____;
②要说明另外的两种粒子是否起到催化作用小组同学设计了如下实验,完成探究活动。
实验步骤 | 实验现象 | 结论 |
a.取一支试管加入5mL5%过氧化氢溶液,然后加入2-3滴稀硫酸 | 溶液几乎没有气泡放出 | 实验证明,起催化作用的是_____ 。 |
b.另取一支试管加入5mL5%过氧化氢溶液,然后加入2-3滴硫酸铜溶液 | 溶液中有大量气泡放出 |