题目内容
85克5%的食盐溶液中,加入15克食盐后成为
- A.100克19.25%的溶液
- B.100克20%的溶液
- C.85克20%的溶液
- D.85克15%的溶液
A
分析:利用溶质质量=溶液质量×溶质的质量分数,溶质质量分数= 100%,结合题意进行分析解答.
100%,结合题意进行分析解答.
解答:85克5%的食盐溶液中,加入15克食盐后,形成溶液的质量为85g+15g=100g,所得溶液的质量分数为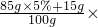 100%=19.25%.
100%=19.25%.
故选A.
点评:本题难度不大,掌握溶质质量分数的有关计算并能灵活运用是正确解答本题的关键.
分析:利用溶质质量=溶液质量×溶质的质量分数,溶质质量分数=
 100%,结合题意进行分析解答.
100%,结合题意进行分析解答.解答:85克5%的食盐溶液中,加入15克食盐后,形成溶液的质量为85g+15g=100g,所得溶液的质量分数为
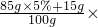 100%=19.25%.
100%=19.25%.故选A.
点评:本题难度不大,掌握溶质质量分数的有关计算并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
下表为NH4Cl、NaCl、KNO3在不同温度下的溶解度,根据表中数据,回答下列问题:
(1)写出NH4Cl和NaCl具有相同溶解度的温度范围(限相邻两个温度之间) ;
(2)60℃时,配制硝酸钾溶液溶质质量分数最大为 ;
(3)若硝酸钾中含有少量氯化钠,应采取的结晶分离方法是 .
(4)20℃取100克NaCl溶液,温度保持不变,若蒸发10克水,则析出1克食盐,若再若蒸发10克水,则会析出晶体 克.
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ | 80℃ | |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 | 65.6 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 |
(2)60℃时,配制硝酸钾溶液溶质质量分数最大为
(3)若硝酸钾中含有少量氯化钠,应采取的结晶分离方法是
(4)20℃取100克NaCl溶液,温度保持不变,若蒸发10克水,则析出1克食盐,若再若蒸发10克水,则会析出晶体
下表是氯化钠和硝酸钾在不同温度下的溶解度S(克/100克水),根据此表回答:
(1)50℃时,硝酸钾的溶解度为85.5克/100克水,表示的含义是 .
(2)在60℃时,10克水中加入12克硝酸钾,充分搅拌后所得溶液的质量为 克,该溶液的溶质质量分数为 .(计算结果精确到0.1%)
(3)由表中数据可知,硝酸钾和氯化钠在某温度范围内溶解度相等,这个温度范围是 .
(4)海水制食盐利用蒸发溶剂的方法,其原理是 .
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| NaCl的溶解度 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 |
| KNO3的溶解度 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 | 138.0 |
(2)在60℃时,10克水中加入12克硝酸钾,充分搅拌后所得溶液的质量为
(3)由表中数据可知,硝酸钾和氯化钠在某温度范围内溶解度相等,这个温度范围是
(4)海水制食盐利用蒸发溶剂的方法,其原理是