题目内容
【题目】某化学兴趣小组通过实验探究分解氯酸钾制氧气的反应中二氧化锰的作用,该反应的符号表达式为______.
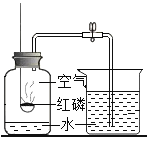
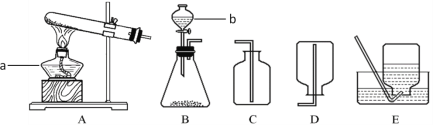
(设计实验)用图 1 所示装置进行实验,步骤如下:
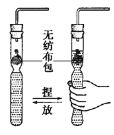
步骤Ⅰ:检查装置气密性,操作方法是______,观察到______,则说明装置气密性良好; 步骤Ⅱ:按照如图 1 装入药品;
步骤Ⅲ:加热右侧支管,用带火星的木条在导管口检验生成的气体; 步骤Ⅳ:冷却后,将装置倾斜,使左侧支管中的药品进入右侧支管,再加热右侧支管,用带火星的木条在导 管口检验生成的气体.
(实验现象)步骤Ⅲ和步骤Ⅳ中,一段时间后都能观察到带火星的木条复燃,但不同的是______.
(交流反思)要想确认分解氯酸钾制氧气的反应中二氧化锰是催化剂,还需通过实验证明二氧化锰的_____和_____在反应前后都没有发生变化.
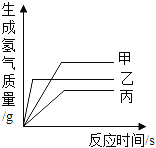
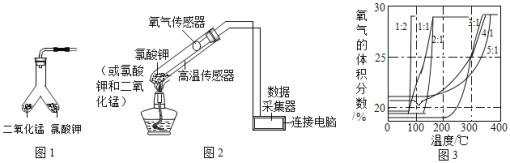
(拓展探究)在老师的指导下,该小组同学利用图 2 所示装置继续进行深入探究.以氧气的体积分数为纵 坐标,温度为横坐标,得到图 3 所示曲线(图中的“1:2”、“1:1”、“2:1”、“3:1”、“4:1”、“5:1”指氯 酸钾和二氧化锰的质量比).
(实 验 分 析) 根据图 3氯酸钾的分解温度随氯酸钾和二氧化锰的质量比变化的大致规律是__________________ ;分解氯酸钾制氧气的反应中二氧化锰起催化作用,可能是因为二氧化锰能_______________________.
【答案】KClO3![]() KCl+O2连接装置,先将导管口伸入液面以下,双手紧握 Y 型试管;导管口有气泡冒出步骤Ⅳ中木条复燃更快质量化学性质氯酸钾和二氧化锰质量比越小,氯酸钾分解温度越低;降低氯酸钾的分解温度
KCl+O2连接装置,先将导管口伸入液面以下,双手紧握 Y 型试管;导管口有气泡冒出步骤Ⅳ中木条复燃更快质量化学性质氯酸钾和二氧化锰质量比越小,氯酸钾分解温度越低;降低氯酸钾的分解温度
【解析】
在二氧化锰的催化作用下,加热氯酸钾分解为氯化钾和氧气;反应的符号表达式为:KClO3 ![]() KCl+O2;
KCl+O2;
【设计实验】
根据图 1的特点,分析可知,检查装置气密性的方法是:连接装置,先将导管口伸入液面以下,双手紧握 Y 型试管,导管口有气泡冒出,证明装置不漏气;
【实验现象】
步骤Ⅲ中是单独加热氯酸钾制取氧气,需要加热的温度较高,加热时间长,所以带火星的木条复燃较慢;步骤Ⅳ中氯酸钾在二氧化锰的催化作用下分解生成氧气,需要的温度较低,分解速率快,所以带火星的木条复燃较快;
【交流反思】
在化学反应里能改变其他物质的化学反应速率(既能提高也能降低),而本身的质量和化学性质在化学反应前后都没有发生改变的物质叫做催化剂,所以步骤Ⅳ的实验现象不能说明MnO2是KClO3分解的催化剂,还需证明在此反应中MnO2的质量和化学性质不变;
【实验分析】
通过分析图3中氯酸钾的分解数据可知,KClO3分解温度随物质配比变化的规律是配比越大,分解温度越高,氯酸钾和二氧化锰的质量比越小,氯酸钾的分解温度越低;分解氯酸钾制氧气的反应中二氧化锰起催化作用,可能是因为二氧化锰能降低氯酸钾的分解温度。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】金属用途广泛,其结构和性质等是化学的重要研究内容.
![]() 如图
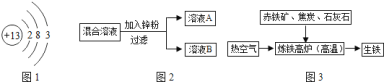
如图![]() 是铝的原子结构示意图.下列说法不正确的是________
是铝的原子结构示意图.下列说法不正确的是________
A.铝原子的质子数为![]()
B.在化合物中铝通常显![]() 价
价
C.铝是地壳中含量最多的元素
D.铝可作导线是由于它具有良好的导电性
![]() 某化学小组用一定量的
某化学小组用一定量的![]() 和
和![]() 混合溶液进行了如图
混合溶液进行了如图![]() 实验,并对溶液
实验,并对溶液![]() 和固体
和固体![]() 的成分进行了分析和研究.
的成分进行了分析和研究.
(提出问题)溶液![]() 中的溶质可能有哪些?
中的溶质可能有哪些?
(做出猜想)①只有![]() ②
②![]() 、
、![]()
③![]() 、
、![]() ④
④![]() 、
、![]() 、
、![]()
(交流讨论)不合理的猜想是________(填标号),其理由是________.
(实验探究)若猜想①成立,通过以下实验可确定固体![]() 的成分,请将下表填写完整.
的成分,请将下表填写完整.
实验步骤 | 现象 | 有关反应的化学方程式 |
取少量固体 | 有气泡产生 | ________ |
![]() 如图
如图![]() 是工业炼铁示意图.其中,焦炭的作用是燃烧提供能量和________;
是工业炼铁示意图.其中,焦炭的作用是燃烧提供能量和________;
![]() 有铁生成的化学方程式为________.
有铁生成的化学方程式为________.
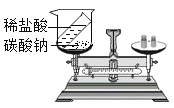
![]() 称取
称取![]() 石灰石(主要成分是
石灰石(主要成分是![]() ,杂质不参与反应)放入烧杯中,向其中加入
,杂质不参与反应)放入烧杯中,向其中加入![]() 稀盐酸,二者恰好完全反应.反应结束后称量烧杯中剩余物质的总质量为
稀盐酸,二者恰好完全反应.反应结束后称量烧杯中剩余物质的总质量为![]() (包括烧杯的质量,且气体的溶解度忽略不计).试计算石灰石中杂质的质量分数_________.
(包括烧杯的质量,且气体的溶解度忽略不计).试计算石灰石中杂质的质量分数_________.
【题目】研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的过程:
【假设】H2O2生成O2的快慢与催化剂种类有关。
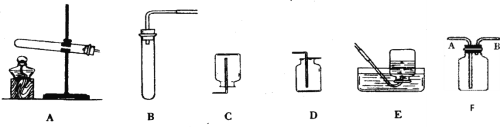
【实验方案】常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入相同质量的MnO2和水泥块,测量各生成一瓶(相同体积)O2所需的时间。
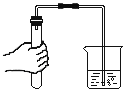
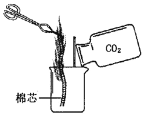
【进行实验】右下图是他们进行实验的装置图,气体发生装置中A仪器的名称是_____________,此实验中B处宜采用的气体收集方法是_______ _____。
【实验记录】
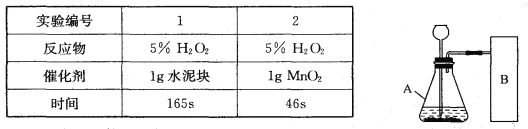
【结论】该探究过程得出的结论是_________________________。
【反思】H2O2在常温下分解缓慢,加入MnO2或水泥块后反应明显加快。若要证明MnO2和水泥块是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的_____ _____是否改变。
【实验拓展】H2O2生成O2的快慢还与哪些因素有关?研究性学习小组进行了更深入的探究:
探究实验一:浓度对化学反应速率的影响
实验步骤 | 现 象 | 结 论 |
取一支试管加入3mL5%的过氧化氢溶液,然后加入少量二氧化锰。 | 缓慢有少量气泡冒出 | |
另取一支试管加入3mL15%的过氧化氢溶液,然后加入少量二氧化锰。 | 迅速有大量气泡冒出 |
请你设计:
实验用品:试管、烧杯、热水、冷水、5%过氧化氢溶液、15%过氧化氢溶液
探究实验二:温度对化学反应速率的影响
实验步骤 | 现 象 | 结 论 |
温度越高,过氧化氢分解的速率越大 |