题目内容
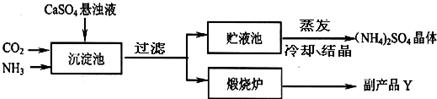
某化工厂为综合利用生产过程中的副产品CaSO4,与相邻的化肥厂联合设计了制备(NH4)2SO4的工艺流程.【工艺流程及原理】

沉淀池中发生的主要化学反应为:CO2+2NH3+CaSO4+H2O=CaCO3↓+(NH4)2SO4
【讨论交流】
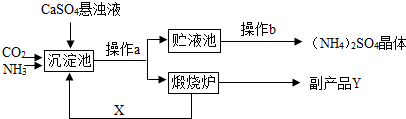
(1)操作a的名称是______,若在实验室进行此操作,用到的玻璃仪器除玻璃棒、烧杯外,还需要______.
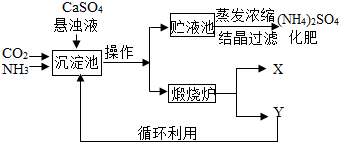
(2)经操作a后得到的固体物质在煅烧炉中高温分解生成X和Y两种物质,该工艺中,Y被作为原料之一循环利用.Y的化学式为______.
(3)沉淀池中也可能生成少量NH4HCO3,该反应的化学方程式为______.
【硫酸铵化肥等级测定】
(1)判断(NH4)2SO4化肥中有无NH4HCO3:
取少量试样溶于水,滴加足量的______,无气泡产生,则可判断该化肥中不存在NH4HCO3.
(2)化肥中氮元素含量的测定(已确定该化肥中不存在NH4HCO3杂质):
【查阅资料】
①已知:(NH4)2SO4+2NaOH
 Na2SO4+2NH3↑+2H2O
Na2SO4+2NH3↑+2H2O氨气极易溶于水,其水溶液为氨水.氨水呈碱性,不稳定,易挥发.
②工业判断硫酸铵化肥等级指标如下:
| 指标 项目 | 优等品 | 合格品 |
| 氮(N)含量 | ≥21.0% | ≥20.5% |
按右图所示装置进行实验.
(1)实验过程中,往烧瓶中加入足量浓氢氧化钠溶液,并加热使硫酸铵充分反应完全转化为NH3.
(2)烧杯中的试剂是为了吸收产生的氨气,下列最适宜的试剂是______(填序号);
①水;②浓HCl;③稀H2SO4;④NaOH溶液
烧杯中干燥管的作用是______.
【交流讨论】
实验小组的同学认为,用上述实验装置测得的结果可能会出现下列情况.
(1)甲同学认为:应在实验装置A、B之间增加一个装有______(填“浓硫酸“或“碱石灰”)的干燥装置,否则实验测得的硫酸铵化肥含氮量可能偏高.
(2)乙同学认为:在实验装置A、B之间增加正确的干燥装置后进行实验,测得的硫酸铵化肥含氮量可能偏低,理由是______.
【实验测定】
经讨论后,他们改进了实验装置,排除了可能产生误差的因素,重新进行实验.
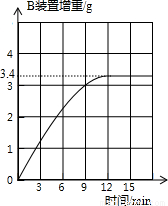
取硫酸铵化肥样品13.5 g进行实验,测得B装置增重与反应时间的关系如右图所示.请通过计算判断该化肥的等级.
计算过程:
该化肥的等级为______品.

【答案】分析:【讨论交流】(1)根据实验的目的确定操作方法,再根据操作方法来确定用到的仪器.
(2)先判断出过滤出来的物质,再分析发生的反应生成物,据图分析出结果.
(3)根据反应物,生成物,反应条件确定化学方程式.
【硫酸铵化肥等级测定】(1)根据碳酸盐的性质,确定碳酸氢氨是否存在.
【实验设计】:(2)从所给试剂的化学物理性质方面确定哪种效果最好;因氨气极易被吸收,要从防止倒吸的角度考虑干燥管的作用.
【交流讨论】:(1)A中可能产生水蒸气,要防止它也作为氨气被吸收;
(2)要使结果准确,还要保证A中的氨气全部被B吸收.
【计算过程】:B增重的质量为生成氨气的质量,根据它算出硫酸铵的质量,再进一步求出样品中硫酸铵的质量分数,判断是否合格.
解答:解:【讨论交流】(1)a操作的目的是把混合物分成固体和液体两部分,要用过滤的操作方法.
(2)过滤后得到的固体物质是碳酸钙,在煅烧炉中高温分解生成氧化钙和二氧化碳两种物质,由图示知,后者是可反复利用.
(3)反应物为氨气及二氧化碳和水,生成物为碳酸氢氨,常温下反应,则方程式为:CO2+NH3+H2O=NH4HCO3.
【硫酸铵化肥等级测定】(1)碳酸氢氨可与酸反应生成二氧化碳气体,有气泡放出现象,所以可加入盐酸(HCl)、硫酸(H2SO4)或硝酸(HNO3)等判断是否存在.
【实验设计】:(2)①水,②浓HCl,③稀H2SO4,④NaOH溶液四种物质中,水不如酸吸收效果好,但盐酸易挥发,不能采用,氢氧化钠与氨气不反应,所以选③;氨气极易和硫酸反应被吸收,要防止倒吸.
【交流讨论】:(1)A中可能产生水蒸气,要防止它也作为氨气被吸收,但浓硫酸不但可吸收水蒸气,也吸收氨气,所以只能用碱石灰;
(2)要使结果准确,还要保证A中的氨气全部被B吸收,图中缺少赶尽反应装置中残留氨气的装置(或有氨气残留在装置中)
【计算过程】:
解:增重的3.4g为氨气的质最.
设13.5g样品中含有(NH4)2SO4的质量为x.
(NH4)2SO4+2NaOH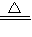 Na2SO4+2NH3↑+2H2O
Na2SO4+2NH3↑+2H2O
132 34
x 3.4g
132:34=x:3.4g
解得:x=13.2g
(14×2)÷132×13.2g=2.8g
2.8g÷13.5g×100%=20.7%
20.5%≤20.7%≤21.0%,为合格品.
故答案为:【讨论交流】(1)过滤;漏斗;(2)CO2;(3)CO2+NH3+H2O=NH4HCO3
【硫酸铵化肥等级测定】(1)盐酸(HCl)、硫酸(H2SO4)或硝酸(HNO3)等;
实验设计:(2)③;防止倒吸;
交流讨论:(1)碱石灰;(2)缺少赶尽反应装置中残留氨气的装置(或有氨气残留在装置中)
计算过程:
解:增重的3.4g为氨气的质最.
设13.5g样品中含有(NH4)2SO4的质量为x.
(NH4)2SO4+2NaOH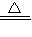 Na2SO4+2NH3↑+2H2O
Na2SO4+2NH3↑+2H2O
132 34
x3.4g
132:34=x:3.4g
解得:x=13.2g
(14×2)/132×13.2g=2.8g
2.8g÷13.5g×100%=20.7%,20.5%≤20.7%≤21.0%,为合格品.
点评:本题为综合型的大实验题,有实验又有计算,做题时要认真审题,要细心,步步为营.
(2)先判断出过滤出来的物质,再分析发生的反应生成物,据图分析出结果.
(3)根据反应物,生成物,反应条件确定化学方程式.
【硫酸铵化肥等级测定】(1)根据碳酸盐的性质,确定碳酸氢氨是否存在.
【实验设计】:(2)从所给试剂的化学物理性质方面确定哪种效果最好;因氨气极易被吸收,要从防止倒吸的角度考虑干燥管的作用.
【交流讨论】:(1)A中可能产生水蒸气,要防止它也作为氨气被吸收;
(2)要使结果准确,还要保证A中的氨气全部被B吸收.
【计算过程】:B增重的质量为生成氨气的质量,根据它算出硫酸铵的质量,再进一步求出样品中硫酸铵的质量分数,判断是否合格.
解答:解:【讨论交流】(1)a操作的目的是把混合物分成固体和液体两部分,要用过滤的操作方法.
(2)过滤后得到的固体物质是碳酸钙,在煅烧炉中高温分解生成氧化钙和二氧化碳两种物质,由图示知,后者是可反复利用.
(3)反应物为氨气及二氧化碳和水,生成物为碳酸氢氨,常温下反应,则方程式为:CO2+NH3+H2O=NH4HCO3.
【硫酸铵化肥等级测定】(1)碳酸氢氨可与酸反应生成二氧化碳气体,有气泡放出现象,所以可加入盐酸(HCl)、硫酸(H2SO4)或硝酸(HNO3)等判断是否存在.
【实验设计】:(2)①水,②浓HCl,③稀H2SO4,④NaOH溶液四种物质中,水不如酸吸收效果好,但盐酸易挥发,不能采用,氢氧化钠与氨气不反应,所以选③;氨气极易和硫酸反应被吸收,要防止倒吸.
【交流讨论】:(1)A中可能产生水蒸气,要防止它也作为氨气被吸收,但浓硫酸不但可吸收水蒸气,也吸收氨气,所以只能用碱石灰;
(2)要使结果准确,还要保证A中的氨气全部被B吸收,图中缺少赶尽反应装置中残留氨气的装置(或有氨气残留在装置中)
【计算过程】:
解:增重的3.4g为氨气的质最.
设13.5g样品中含有(NH4)2SO4的质量为x.
(NH4)2SO4+2NaOH
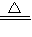 Na2SO4+2NH3↑+2H2O
Na2SO4+2NH3↑+2H2O132 34
x 3.4g
132:34=x:3.4g
解得:x=13.2g
(14×2)÷132×13.2g=2.8g
2.8g÷13.5g×100%=20.7%
20.5%≤20.7%≤21.0%,为合格品.
故答案为:【讨论交流】(1)过滤;漏斗;(2)CO2;(3)CO2+NH3+H2O=NH4HCO3
【硫酸铵化肥等级测定】(1)盐酸(HCl)、硫酸(H2SO4)或硝酸(HNO3)等;
实验设计:(2)③;防止倒吸;
交流讨论:(1)碱石灰;(2)缺少赶尽反应装置中残留氨气的装置(或有氨气残留在装置中)
计算过程:
解:增重的3.4g为氨气的质最.
设13.5g样品中含有(NH4)2SO4的质量为x.
(NH4)2SO4+2NaOH
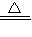 Na2SO4+2NH3↑+2H2O
Na2SO4+2NH3↑+2H2O132 34
x3.4g
132:34=x:3.4g
解得:x=13.2g
(14×2)/132×13.2g=2.8g
2.8g÷13.5g×100%=20.7%,20.5%≤20.7%≤21.0%,为合格品.
点评:本题为综合型的大实验题,有实验又有计算,做题时要认真审题,要细心,步步为营.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
某化学研究性学习小组参加社会社会实践调查得知:某化工厂为综合利用生产过程中的副产品CaSO4,与相邻的化肥厂联合设计了以下制备(NH4)2SO4的工艺流程.
[工艺流程示意图]
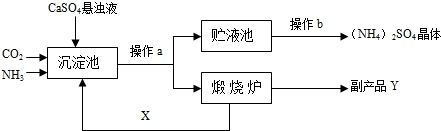
上述流程中,沉淀池中发生的主要化学反应为:CO2+2NH3+CaSO4+H2O=CaCO3↓+(NH4)2SO4
[讨论交流]
(1)操作a的名称是 ,实验室中进行此操作时,用到的玻璃仪器除玻璃棒、烧杯外,还需要 .
(2)经操作a后得到的某物质在煅烧炉中发生反应的化学方程式为 .该工艺中,X在沉淀池中被消耗,在煅烧炉中又生成,故X可循环使用.X的填化学式为 .
(3)图中操作b应怎样进行呢?
查阅资料:右图是硫酸铵在水中的溶解度曲线.
表:固体硫酸铵在部分温度时的溶解度.
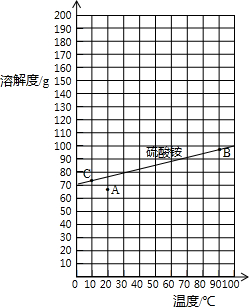
下列说法正确的有 .
①从溶解度曲线中,可以查找70℃时硫酸铵的溶解度约90g;②图中的A点表示硫酸铵溶液的状态不饱和;③若将A点变成B点的操作采用加热蒸发、使溶液浓缩的方法④若将B点转化为C点时,采用的是冷却热饱和溶液方法
该化肥厂生产的硫酸铵化肥品质怎样呢?
[查阅资料]下表是硫酸铵化肥品质的主要指标.
氨气极易溶于水,其水溶液为氨水,呈碱性.
已知:(NH4)2SO4+2NaOH
Na2SO4+2NH3↑+2H2O
[观察外观]该硫酸铵化肥无可见机械杂质.
[实验探究]按如图所示装置进行实验.
(1)实验过程中,为使硫酸铵充分反应完全转化为NH3,则需往烧瓶中加入足量浓氢氧化钠溶液并充分加热.
(2)选择右图装置A进行实验的原因 ,烧杯中盛放的试剂稀硫酸可以吸收氨气,两者化合生成一种盐,写出化学方程式 .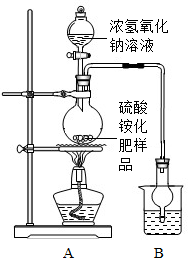
[交流讨论]
甲同学认为:应在实验装置中A、B装置间加装一个干燥装置,否则根据实验测得的数据,计算硫酸铵化肥的含氮量可能 (填“偏高”或“偏低”).
乙同学认为:改进后的实验装置中还存在另一个明显缺陷是: .
(经过大家充分讨论后,对实验装置进行了改进,重新进行实验.)
[探究结论]称取13.5 g硫酸铵化肥样品,用最终改进后的实验装置重新进行实验,经数据处理释放出氨气的质量与反应时间如图所示.试通过计算,判断该化肥的等级. (要求写出计算过程)
[工艺流程示意图]

上述流程中,沉淀池中发生的主要化学反应为:CO2+2NH3+CaSO4+H2O=CaCO3↓+(NH4)2SO4
[讨论交流]
(1)操作a的名称是
(2)经操作a后得到的某物质在煅烧炉中发生反应的化学方程式为
(3)图中操作b应怎样进行呢?
查阅资料:右图是硫酸铵在水中的溶解度曲线.
表:固体硫酸铵在部分温度时的溶解度.
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 溶解度/g | 70.6 | 73 | 75.4 | 78 | 81 | 85 | 88 | ? | 95 | 98 | 103 |

下列说法正确的有
①从溶解度曲线中,可以查找70℃时硫酸铵的溶解度约90g;②图中的A点表示硫酸铵溶液的状态不饱和;③若将A点变成B点的操作采用加热蒸发、使溶液浓缩的方法④若将B点转化为C点时,采用的是冷却热饱和溶液方法
该化肥厂生产的硫酸铵化肥品质怎样呢?
[查阅资料]下表是硫酸铵化肥品质的主要指标.
| 指标项目 | 优等品 | 一等品 | 合格品 |
| 外观 | 白色结晶,无可见机械杂质 | 无可见机械杂质 | |
| 氮(N)含量 | ≥21.0% | ≥20.7% | ≥20.5% |
已知:(NH4)2SO4+2NaOH
| ||
[观察外观]该硫酸铵化肥无可见机械杂质.
[实验探究]按如图所示装置进行实验.
(1)实验过程中,为使硫酸铵充分反应完全转化为NH3,则需往烧瓶中加入足量浓氢氧化钠溶液并充分加热.
(2)选择右图装置A进行实验的原因

[交流讨论]
甲同学认为:应在实验装置中A、B装置间加装一个干燥装置,否则根据实验测得的数据,计算硫酸铵化肥的含氮量可能
乙同学认为:改进后的实验装置中还存在另一个明显缺陷是:
(经过大家充分讨论后,对实验装置进行了改进,重新进行实验.)
[探究结论]称取13.5 g硫酸铵化肥样品,用最终改进后的实验装置重新进行实验,经数据处理释放出氨气的质量与反应时间如图所示.试通过计算,判断该化肥的等级.