题目内容
若6g某物质在空气中完全燃烧生成8.8g二氧化碳和3.6g水(只有这两种产物),则关于这种物质的描述正确的是( )A.该物质由碳、氢两种元素组成
B.该物质由碳、氢、氧三种元素组成
C.该物质碳,氢元素的质量比为4:1
D.该物质分子中碳,氧原子个数比为1:1
【答案】分析:6g某物质在空气中完全燃烧生成8.8g二氧化碳和3.6g水,根据质量守恒定律,生成的8.8g二氧化碳中的碳元素和3.6g水中氢元素均来自于6g的某物质,利用碳、氢元素的质量及某物质的质量,进行分析判断即可.
解答:解:8.8g二氧化碳中碳元素的质量=8.8g×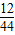 ×100%=2.4g;3.6g水中氢元素的质量=3.6g×
×100%=2.4g;3.6g水中氢元素的质量=3.6g×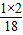 ×100%=0.4g;
×100%=0.4g;
A、由质量守恒定律,该物质中碳、氢元素质量和=2.4g+0.4g=2.8g,小于该物质的质量6g,因此该物质中除碳、氢元素外还应含有氧元素(其质量为6g-2.8g=3.2g),故选项说法错误.
B、由A选项的分析,该物质是由碳、氢、氧三种元素组成的,故选项说法正确.
C、该物质中碳、氢元素质量比=2.4g:0.4g=6:1,故选项说法错误.
D、碳元素和氧元素的质量比为2.4g:3.2g=3:4,碳元素和氧元素的相对原子质量为12和16,则该物质的分子中碳原子与氢原子的个数比=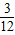 :
: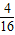 =1:1,故选项说法正确.
=1:1,故选项说法正确.
故选BD.
点评:本题难度不大,掌握质量守恒定律、化合物中某元素的质量=该化合物的质量×该元素的质量分数并能灵活运用是正确解答本题的关键.
解答:解:8.8g二氧化碳中碳元素的质量=8.8g×
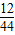 ×100%=2.4g;3.6g水中氢元素的质量=3.6g×
×100%=2.4g;3.6g水中氢元素的质量=3.6g×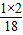 ×100%=0.4g;
×100%=0.4g;A、由质量守恒定律,该物质中碳、氢元素质量和=2.4g+0.4g=2.8g,小于该物质的质量6g,因此该物质中除碳、氢元素外还应含有氧元素(其质量为6g-2.8g=3.2g),故选项说法错误.
B、由A选项的分析,该物质是由碳、氢、氧三种元素组成的,故选项说法正确.
C、该物质中碳、氢元素质量比=2.4g:0.4g=6:1,故选项说法错误.
D、碳元素和氧元素的质量比为2.4g:3.2g=3:4,碳元素和氧元素的相对原子质量为12和16,则该物质的分子中碳原子与氢原子的个数比=
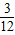 :
: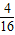 =1:1,故选项说法正确.
=1:1,故选项说法正确.故选BD.
点评:本题难度不大,掌握质量守恒定律、化合物中某元素的质量=该化合物的质量×该元素的质量分数并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目