题目内容
实验室常用下列装置来制取氧气:

(1)用A图制取氧气前检验装置气密性的常用方法是
(2)用高锰酸钾制取氧气时发生反应的化学方程式为
若用排水法收集氧气,判断氧气收集满的方法是
(3)实验室常用碳酸钙固体与稀盐酸来制取二氧化碳.常温下二氧化碳的密度比空气大,可溶于水.应该从上图中选择的发生装置是

(1)用A图制取氧气前检验装置气密性的常用方法是
先将导管的一端浸入水中,再用手紧握试管,观察到烧杯内导管口有气泡冒出或冷却后看导管口是否形成一段水柱,证明气密性良好
先将导管的一端浸入水中,再用手紧握试管,观察到烧杯内导管口有气泡冒出或冷却后看导管口是否形成一段水柱,证明气密性良好
.(2)用高锰酸钾制取氧气时发生反应的化学方程式为
2KMnO4
K2MnO4+MnO2+O2↑
| ||
2KMnO4
K2MnO4+MnO2+O2↑
.
| ||
若用排水法收集氧气,判断氧气收集满的方法是
当在瓶口看到有连续气泡冒出,说明已收满
当在瓶口看到有连续气泡冒出,说明已收满
.(3)实验室常用碳酸钙固体与稀盐酸来制取二氧化碳.常温下二氧化碳的密度比空气大,可溶于水.应该从上图中选择的发生装置是
B
B
,收集装置是E
E
.分析:(1)根据检查装置气密性的方法及注意事项分析即可.装置气密性检验的原理是:通过气体发生器与附设的液体构成封闭体系,依据改变体系内压强时产生的现象(如气泡的生成、水柱的形成、液面的升降等)来判断装置气密性的好坏.
(2)根据高锰酸钾加热制氧气的反应原理并结合方程式的书写步骤书写方程式.用排水法收集时,当看到瓶口有连续气泡时,说明已收满.
(3)是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.
(2)根据高锰酸钾加热制氧气的反应原理并结合方程式的书写步骤书写方程式.用排水法收集时,当看到瓶口有连续气泡时,说明已收满.
(3)是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.
解答:解:(1)检验装置气密性的方法是:先将导管的一端浸入水中,再用手紧握试管,观察到烧杯内导管口有气泡冒出或冷却后看导管口是否形成一段水柱,证明气密性良好;
(2)高锰酸钾加热生成锰酸钾、二氧化锰和氧气,方程式是2KMnO4
K2MnO4+MnO2+O2↑;用排水法收集氧气,开始集气瓶中装满水后倒扣在水槽中,产生的氧气将水排除,当在瓶口看到有连续气泡冒出,说明已收满;
(3)实验室制取CO2,是在常温下,用碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,因此不需要加热,所以选用B发生装置.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.
故答案为:(1)先将导管的一端浸入水中,再用手紧握试管,观察到烧杯内导管口有气泡冒出或冷却后看导管口是否形成一段水柱,证明气密性良好
(2)2KMnO4
K2MnO4+MnO2+O2↑;当在瓶口看到有连续气泡冒出,说明已收满
(3)B;E
(2)高锰酸钾加热生成锰酸钾、二氧化锰和氧气,方程式是2KMnO4
| ||
(3)实验室制取CO2,是在常温下,用碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,因此不需要加热,所以选用B发生装置.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.
故答案为:(1)先将导管的一端浸入水中,再用手紧握试管,观察到烧杯内导管口有气泡冒出或冷却后看导管口是否形成一段水柱,证明气密性良好
(2)2KMnO4
| ||
(3)B;E
点评:本考点主要考查了检查装置的气密性、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目

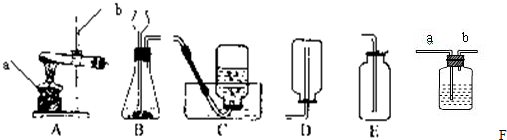

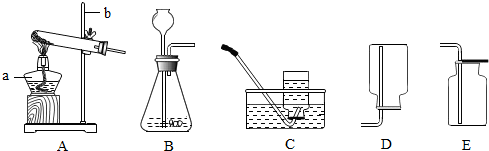
 实验室常用下列装置来制取氧气:
实验室常用下列装置来制取氧气: