ΧβΡΩΡΎ»ί
ΡΩ«Α άΫγ…œ60%ΒΡΟΨ «¥”ΚΘΥ°÷–Χα»ΓΒΡΘ°ΚΘΥ°ΧαΟΨΒΡ÷ς“ΣΝς≥Χ»γœ¬ΘΚ
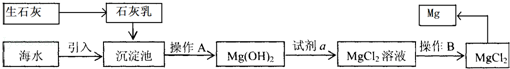
Θ®1Θ©œρΚΘΥ°÷–Φ”»κ ·Μ“»ιΒΡΉς”Ο « Θ°
Θ®2Θ©¥”≥δΖ÷άϊ”ΟΚΘ―σΜ·―ßΉ ‘¥ΓΔΧαΗΏΨ≠ΦΟ–ß“φΒΡΫ«Ε»Θ§…ζ≤ζ…ζ ·Μ“ΒΡ÷ς“Σ‘≠Νœά¥‘¥”ΎΚΘ―σ÷–ΒΡ±¥Ω«Θ§…ζ ·Μ“ΚΆΥ°Ζ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ « Θ°
Θ®3Θ©≤ΌΉςA « Θ§Φ”»κΒΡΉψΝΩ ‘ΦΝa « Θ®ΧνΜ·―ß ΫΘ©Θ°
Θ®4Θ©“―÷ΣMgCl2ΒΡ»ήΫβΕ»ΥφΈ¬Ε»ΒΡ…ΐΗΏΕχ‘ω¥σΘ°œ¬Ν–ΗςΆΦ «Ρ≥MgCl2±ΞΚΆ»ή“ΚΒΡ≈®Ε»ΥφΈ¬Ε»…ΐΗΏΕχ±δΜ·ΒΡΆΦœσΘ®≤ΜΩΦ¬«»ήΦΝΒΡ÷ ΝΩ±δΜ·Θ©Θ§Τδ÷–’ΐ»ΖΒΡ «ΓΓ ΓΓ
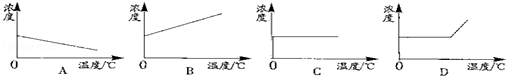
Θ®5Θ©ΚΘΥ°ΧαΟΨΒΡΙΐ≥Χ÷–Θ§ΫΪΚΘΥ°÷–ΒΡ¬»Μ·ΟΨΉΣ±δΈΣ«β―θΜ·ΟΨΘ§‘ΌΉΣ±δΈΣ¬»Μ·ΟΨΒΡ‘≠“ρ «ΘΚ Θ°
Θ®6Θ© ‘ΦΝaΨΏ”–¥ΧΦΛ–‘ΤχΈΕΘ§Έ“Ο«Η’Ϋχ Β―ι “ΨΆΡήΈ≈ΒΫ’β÷÷ΤχΈΕΘ§ΥΒΟςΖ÷Ή”ΒΡ–‘÷ «ΘΚ Θ°

Θ®1Θ©œρΚΘΥ°÷–Φ”»κ ·Μ“»ιΒΡΉς”Ο « Θ°
Θ®2Θ©¥”≥δΖ÷άϊ”ΟΚΘ―σΜ·―ßΉ ‘¥ΓΔΧαΗΏΨ≠ΦΟ–ß“φΒΡΫ«Ε»Θ§…ζ≤ζ…ζ ·Μ“ΒΡ÷ς“Σ‘≠Νœά¥‘¥”ΎΚΘ―σ÷–ΒΡ±¥Ω«Θ§…ζ ·Μ“ΚΆΥ°Ζ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ « Θ°
Θ®3Θ©≤ΌΉςA « Θ§Φ”»κΒΡΉψΝΩ ‘ΦΝa « Θ®ΧνΜ·―ß ΫΘ©Θ°
Θ®4Θ©“―÷ΣMgCl2ΒΡ»ήΫβΕ»ΥφΈ¬Ε»ΒΡ…ΐΗΏΕχ‘ω¥σΘ°œ¬Ν–ΗςΆΦ «Ρ≥MgCl2±ΞΚΆ»ή“ΚΒΡ≈®Ε»ΥφΈ¬Ε»…ΐΗΏΕχ±δΜ·ΒΡΆΦœσΘ®≤ΜΩΦ¬«»ήΦΝΒΡ÷ ΝΩ±δΜ·Θ©Θ§Τδ÷–’ΐ»ΖΒΡ «ΓΓ ΓΓ

Θ®5Θ©ΚΘΥ°ΧαΟΨΒΡΙΐ≥Χ÷–Θ§ΫΪΚΘΥ°÷–ΒΡ¬»Μ·ΟΨΉΣ±δΈΣ«β―θΜ·ΟΨΘ§‘ΌΉΣ±δΈΣ¬»Μ·ΟΨΒΡ‘≠“ρ «ΘΚ Θ°
Θ®6Θ© ‘ΦΝaΨΏ”–¥ΧΦΛ–‘ΤχΈΕΘ§Έ“Ο«Η’Ϋχ Β―ι “ΨΆΡήΈ≈ΒΫ’β÷÷ΤχΈΕΘ§ΥΒΟςΖ÷Ή”ΒΡ–‘÷ «ΘΚ Θ°
Θ®1Θ© ΙMg2+–Έ≥…MgΘ®OHΘ©2≥ΝΒμΘ°
Θ®2Θ©CaO+H2O®TCaΘ®OHΘ©2Θ°
Θ®3Θ©Ιΐ¬ΥΘΜHClΘ°
Θ®4Θ©C
Θ®5Θ©ΚΘΥ°÷–¬»Μ·ΟΨΒΡΚ§ΝΩΚή¥σΘ§ΒΪΟΨάκΉ”≈®Ε»ΚήΒΆΘ§ΗΟΙΐ≥ΧΩ…“‘ ΙΟΨάκΉ”ΗΜΦ·Θ§≈®Ε»ΗΏΘ§«“≥…±ΨΒΆΘ°
Θ®6Θ©Ζ÷Ή”‘Ύ”ά≤ΜΆΘœΔΒΊΉωΈόΙφ¬…‘ΥΕ·Θ°
Θ®2Θ©CaO+H2O®TCaΘ®OHΘ©2Θ°
Θ®3Θ©Ιΐ¬ΥΘΜHClΘ°
Θ®4Θ©C
Θ®5Θ©ΚΘΥ°÷–¬»Μ·ΟΨΒΡΚ§ΝΩΚή¥σΘ§ΒΪΟΨάκΉ”≈®Ε»ΚήΒΆΘ§ΗΟΙΐ≥ΧΩ…“‘ ΙΟΨάκΉ”ΗΜΦ·Θ§≈®Ε»ΗΏΘ§«“≥…±ΨΒΆΘ°
Θ®6Θ©Ζ÷Ή”‘Ύ”ά≤ΜΆΘœΔΒΊΉωΈόΙφ¬…‘ΥΕ·Θ°
‘ΧβΖ÷ΈωΘΚΘ®1Θ©ΟΨάκΉ”Ρή”κ«β―θΗυάκΉ”Ζ¥”Π…ζ≥…«β―θΜ·ΟΨ≥ΝΒμΘΚMg2++2OH©¹=MgΘ®OHΘ©2ΓΐΘ§
Θ®2Θ©…ζ ·Μ“ΚΆΥ°Ζ¥”Π…ζ≥… λ ·Μ“Θ§Ζ¥”ΠΖΫ≥Χ Ϋ «CaO+H2O®TCaΘ®OHΘ©2Θ°
Θ®3Θ©Ζ÷άκ≤Μ»ή”ΎΥ°ΒΡΙΧΧεΚΆ“ΚΧεΘ§Ω…”ΟΙΐ¬ΥΒΡΖΫΖ®Θ§¥”≥ΝΒμ≥Ί÷–ΒΟΒΫ«β―θΜ·ΟΨ”ΟΙΐ¬ΥΒΡΖΫΖ®ΘΜ
¥”«β―θΜ·ΟΨΒΫ¬»Μ·ΟΨΘ§«β―θΜ·ΟΨΚΆ―ΈΥαΖ¥”ΠΒΟΒΫ¬»Μ·ΟΨΚΆΥ°Θ§Ζ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣΘΚMgΘ®OHΘ©2+2HCl=MgCl2+2H2OΘ§Φ”»κΒΡΉψΝΩ ‘ΦΝa «HClΘ§
Θ®4Θ©ΫΪMgCl2±ΞΚΆ»ή“ΚΦ”»»ΚσΘ§Υδ»Μ»ή“Κ”…±ΞΚΆ±δΈΣ≤Μ±ΞΚΆΘ§ΒΪ»ή÷ ΒΡ÷ ΝΩ”κ»ήΦΝ≤ΔΈ¥ΗΡ±δΘ§Υυ“‘»ή÷ ÷ ΝΩΖ÷ ΐΘ®Φ¥≈®Ε»Θ©ΥφΉ≈Έ¬Ε»ΒΡ…ΐΗΏ≤ΔΈ¥ΗΡ±δΘ°
Θ®5Θ©ΫΪΚΘΥ°÷–ΒΡ¬»Μ·ΟΨΚ§ΝΩ¥σΘ§”…”ΎΈ¥ΗΜΦ·Θ§ΟΨάκΉ”≈®Ε»ΚήΒΆΘ§÷±Ϋ”Φ”»»≈®ΥθΧα»Γ–κœϊΚΡ¥σΝΩΒΡΒγΡήΘ§≥…±ΨΗΏΘ§«“Χα»ΓΒΡ¬»Μ·ΟΨ―Έ÷–Μλ”–¥σΝΩΒΡΤδΥϋ¬»Μ·ΡΤ―ΈΒ»άκΉ”Θ§Υυ“‘–κΫΪΚΘΥ°÷–ΒΡ¬»Μ·ΟΨΉΣ±δΈΣ«β―θΜ·ΟΨΘ§‘ΌΉΣ±δΈΣ¬»Μ·ΟΨΘ§
Θ®6Θ© ‘ΦΝaΨΏ”–¥ΧΦΛ–‘ΤχΈΕΘ§Έ“Ο«Η’Ϋχ Β―ι “ΨΆΡήΈ≈ΒΫ’β÷÷ΤχΈΕΘ§ «“ρΈΣΖ÷Ή”‘Ύ”ά≤ΜΆΘœΔΒΊΉωΈόΙφ¬…‘ΥΕ·Θ°

ΝΖœΑ≤αœΒΝ–¥πΑΗ
œύΙΊΧβΡΩ


