题目内容
【题目】废旧金属可回收利用,某化学兴趣小组用合金废料(含Fe、Cu和Al)制取FeSO4溶液和回收金属铜,实验流程如图所示(部分生成物已略去)。已知:2Al+2NaOH+2H2O═2NaAlO2+3H2↑
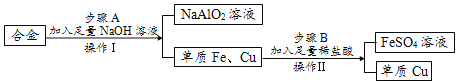
(1)单质铁的金属活动性比铜_____(填“强”或“弱”);
(2)操作Ⅰ的名称_____,操作Ⅱ用到的玻璃仪器有烧杯、玻璃棒和_____(填仪器名称);
(3)若取FeSO4溶液适量,滴入BaCl2溶液,发生反应的化学方程式为_____,该反应属于基本反应类型中的_____反应;
(4)步骤B的化学方程式为_____;
(5)铝制品在空气中耐腐蚀的原因是_____。
【答案】强 过滤 漏斗 FeSO4+BaCl2=BaSO4↓+FeCl2 复分解 Fe+H2SO4=FeSO4+H2↑ 铝在空气中会形成致密的保护膜,阻止铝制品进一步被氧化;
【解析】
(1)在金属活动性顺序中,铁的金属活动性比铜强;
(2)操作Ⅰ、Ⅱ用于分离固体和液体,其操作的名称为过滤,操作Ⅱ用到的玻璃仪器有烧杯、玻璃棒和漏斗;
(3)若取FeSO4溶液适量,滴入BaCl2溶液,硫酸亚铁和氯化钡反应生成硫酸钡沉淀和氯化亚铁,发生反应的化学方程式为FeSO4+BaCl2=BaSO4↓+FeCl2,该反应是两种化合物交换成分,生成另外两种化合物,属于复分解反应;
(4)步骤B发生的反应是铁和稀硫酸反应生成硫酸亚铁和氢气,化学方程式为:Fe+H2SO4=FeSO4+H2↑;
(5)在空气中铝制品更耐腐蚀的原因是铝在空气中会形成致密的保护膜,阻止铝制品进一步被氧化。

练习册系列答案
相关题目