题目内容
【题目】化学是在原子、分子水平上研究物质及其变化的科学。
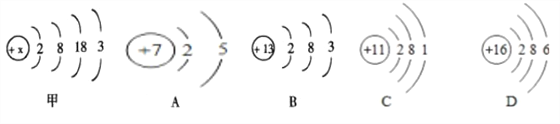
(1)已知镓( Ga)的原子结构示意图如下图(甲)所示,则 x 的值为_____;
(2)镓元素的化学性质与下列哪种元素的化学性质最相似_____(在 A、B、C、D 图 中选择,填字母);
(3)A、B、C、D 图示的四种元素最本质的区别是_____;
(4)镓( Ga)与下图中 A 元素形成的化合物化学式为_____;
(5)D 的离子结构示意图是_____,C 和 D 这两种元素组成的化合物是由
_____(填“原子”、“分子”或“离子”)保持化学性质的。
【答案】 31 B 它们的质子数不同 GaN ![]() 离子
离子
【解析】【试题分析】本题主要考查原子结构示意图的意义,由题目给出信息,推断该元素的原子构成,并对原子构成规律的应用是解题的关键.
(1)原子中核电荷数等于核外电子数,故X=2+8+18+3=31;
(2)元素的化学性质主要决定于该元素原子的最外层电子数。镓元素原子的最外层电子数为3与B原子的最外层电子数相同,所发镓的化学性质与B元素的化学性质最相似;
(3)元素最本质的区别是核电荷数(质子数)不同;
(4)镓的最外层电子数为3,失去3个电子达到稳定结构,氮原子的最外层电子数为5,得到3个电子达到稳定结构,所以镓元素与氮元素结合时原子个数比为1:1时双方都达到了稳定结构。故镓元素与氮元素结合时形成的化合物化学式为GaN;
(5)D原子的最外层电子数为6,形成离子时要得到2个电子才能形成稳定结构,故离子结构示意图是![]() ,C 和 D 这两种元素组成的化合物时,通过得失电子可达到稳定结构,形成的化合物是由离子构成的。故保持物质化学性质的微粒是离子。
,C 和 D 这两种元素组成的化合物时,通过得失电子可达到稳定结构,形成的化合物是由离子构成的。故保持物质化学性质的微粒是离子。

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案
相关题目