题目内容
【题目】老师从实验桌上拿出两瓶常用的但标签已经模糊不清的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体。我们对此气体展开了一系列探究:
(1)猜想:我认为产生的气体能使带火星的木条复燃,我能写出此反应的化学方程式: ,我知道它的反应类型是 。
(2)制取该气体,将选取下图中的发生装置 (填序号,以下同),收集装置 。
(3)如果用下图中的F装置收集该气体,我认为气体应从 端(填“A”或“B”)导入,因为 。
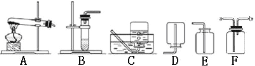
(4)实验室用高锰酸钾制取氧气时,可选用的发生装置是 (填字母代号)。其化学方程式为
(5)实验室制取二氧化碳时,选取图中的装置组合 。如何验满怎样验证
【答案】(1)2H2O2![]() 2H2O+O2↑;分解反应(2)B;C或E
2H2O+O2↑;分解反应(2)B;C或E
(3)A;O2密度比空气大(4)A;2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
(5)B、E;将燃着的木条放在瓶口熄灭,证明已满.。将气体通入澄清石灰水变浑浊,则证明是CO2
【解析】
试题分析∶由题中信息和所学知识知,(1)猜想:我认为产生的气体能使带火星的木条复燃,我能写出此反应的化学方程式:2H2O2![]() 2H2O+O2↑。我知道它的反应类型是分解反应。(2)制取该气体,将选取下图中的发生装置B.收集装置C或E.(3)如果用下图中的F装置收集该气体,我认为气体应从A端导入,因为O2密度比空气大.(4)实验室用高锰酸钾制取氧气时,可选用的发生装置是A.其化学方程式为2KMnO4
2H2O+O2↑。我知道它的反应类型是分解反应。(2)制取该气体,将选取下图中的发生装置B.收集装置C或E.(3)如果用下图中的F装置收集该气体,我认为气体应从A端导入,因为O2密度比空气大.(4)实验室用高锰酸钾制取氧气时,可选用的发生装置是A.其化学方程式为2KMnO4![]() K2MnO4+MnO2+O2↑.(5)实验室制取二氧化碳时,选取图中的装置组合B、E.如何验满∶将燃着的木条放在瓶口熄灭,证明已满.。怎样验证∶将气体通入澄清石灰水变浑浊,则证明是CO2。
K2MnO4+MnO2+O2↑.(5)实验室制取二氧化碳时,选取图中的装置组合B、E.如何验满∶将燃着的木条放在瓶口熄灭,证明已满.。怎样验证∶将气体通入澄清石灰水变浑浊,则证明是CO2。
考点∶考查实验探究的基本思路和方法。

 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案【题目】下列实验现象的描述中,正确的是
A.铜绿加热,试管内壁出现水珠,生成黑色的氧化铜
B.石蜡在氧气中燃烧,发出红光
C.红磷在空气中燃烧产生大量的白雾
D.镁条在空气中燃烧,发出耀眼的白光,生成白色固体
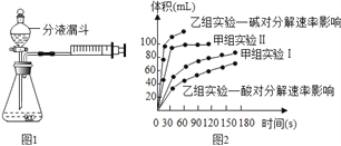
【题目】现甲、乙两化学小组安装两套如图1的相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素。
(1)下列方法能检查该装置气密性的是 。
A、将注射器活塞固定,向分液漏斗中注入适量蒸馏水,打开分液漏斗活塞,如果分液漏斗颈部能形成稳定的水柱,则气密性良好,反之气密性差。
B、关闭分液漏斗活塞,加热锥形瓶,如果注射器活塞外移(右移),停止加热后注射器活塞回到原来位置,则气密性良好,反之气密性差。
C、关闭分液漏斗活塞,用力将注射器活塞外移(右移),停止用力后,注射器活塞不移动,则气密性良好,反之气密性差。
(2)二氧化锰催化下过氧化氢分解的文字或符号表达式是 。
(3)甲小组有如下实验设计方案,完成下表
实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 |
甲组实验Ⅰ | 探究 对 过氧化氢分解速率的影响 | 25℃ | 二氧化锰 | 10mL 2%过氧化氢 |
甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%过氧化氢 |
(4)甲、乙两小组得出如图2的数据
Ⅰ甲组实验得出的数据可知:浓度越大,过氧化氢分解速率 ;(填“越快”或“越慢”)
Ⅱ由乙组研究的酸、碱对过氧化氢分解影响因素的数据分析:相同条件下,过氧化氢在 (填“酸”或“碱”)性环境下放出气体速率较快。
