题目内容
【题目】中和反应在工农业生产中应用广泛,现向40g 10%的氢氧化钠溶液中不断滴加盐酸,同时测定溶液pH的变化(曲线如图),请分析计算: 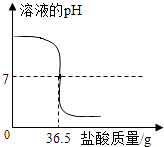
(1)40g 10%的氢氧化钠溶液中含有g的氢氧化钠;当滴入36.5g盐酸时,溶液的pH为 .
(2)所用盐酸的溶质质量分数(写出计算过程).
【答案】
(1)4;7
(2)解:设稀盐酸中溶质的质量为x,
NaOH+ | HCl═NaCl+H2O |
40 | 36.5 |
4g | x |
![]()
x=3.65g
所用盐酸的溶质质量分数= ![]() =10%
=10%
答案:所用盐酸的溶质质量分数为10%
【解析】解:(1)40g 10%的氢氧化钠溶液中含有氢氧化钠的质量为:40g×10%=4g;根据图象可以看出,开始时溶液呈碱性,pH大于7,向氢氧化钠溶液中加入盐酸,盐酸为酸,显酸性,其pH减小,当滴入36.5g盐酸时,溶液的pH为7;
【考点精析】认真审题,首先需要了解根据化学反应方程式的计算(各物质间质量比=系数×相对分子质量之比).

练习册系列答案
相关题目