题目内容
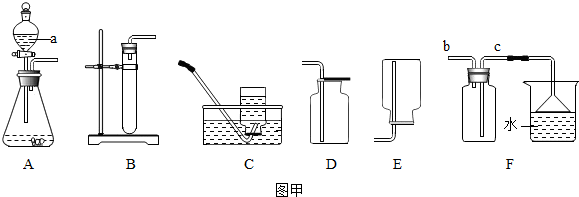
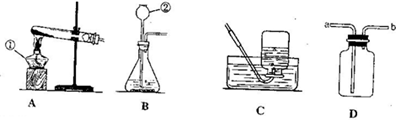
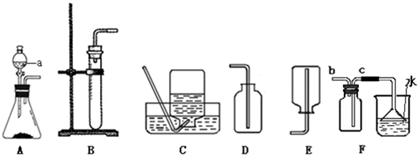
(7分)通过半年的化学学习,你已经掌握了实验室制取气体的有关规律,以下是老师提供的一些实验装置。根据下图及描述回答下列问题:
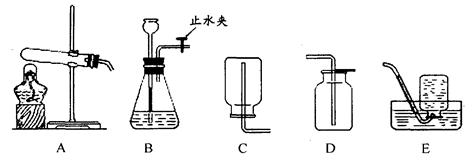
(1)关闭B装置中的止水夹后,从长颈漏斗向锥形瓶中注入一定量的水,静止后如图所示,则B装置是否漏气? (填“漏气”、“不漏气”或“无法确定”)。
(2)写出实验室用B装置制取二氧化碳的化学方程式 。小明同学在一本参考书上发现,镁也能在二氧化碳中燃烧,于是他将镁条点燃后迅速伸入盛有二氧化碳的集气瓶中,发现镁条剧烈燃烧,发出白光,放大量的热,产生一种白色粉末和一种黑色粉末。根据上述现象,写出该反应的化学方程式: 。这个实验还引发了我们对过去某些知识的反思,从而有了新的发现,你认为新的发现是(填序号) ;
①燃烧不一定需要有氧气
②活泼金属着火时不能用二氧化碳灭火
③在一定的条件下,二氧化碳也能支持燃烧
(3)实验室常用加热氯化铵与氢氧化钙固体混合物的方法制取氨气,通常情况下,氨气的密度比空气小且极易溶于水,其水溶液称为氨水;若要制得氨气,应选用的发生装置和收集装置是 (填字母)。小雯同学将收集满氨气的集气瓶倒扣在滴有无色酚酞的水中,观察到的现象是 。
(1)不漏气
(2)CaCO3+2HCl=CaCl2+CO2↑+H2O 2Mg+CO2 2MgO+C ①②③
2MgO+C ①②③
(3)AC 集气瓶内液面上升 溶液变为红色
【解析】
试题分析:(1)根据气密性检查的原理分析,若装置漏气,则装置内的气体会向外逸出,故装置内的气体压强减小,在外界大气压的作用下,长颈漏斗内的液面将会下降,而现在装置内的液面没有下降,说明装置不漏气。
(2)选择制取气体的发生装置,要根据反应物的状态和反应条件,由于装置B是在常温的条件下,用固液体反应来制取气体的装置,所以要制取二氧化碳,需要选择石灰石或大理石和稀盐酸反应,生成二氧化碳气体,故该反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O。根据题意分析,反应物为镁和二氧化碳,生成物为一黑一白两种固体,依据反应前后元素种类不变,可知此两种固体是由镁元素、碳元素和氧元素组成的;再结合所学知识可知,黑色固体应为碳单质,白色固体则为氧化镁,反应条件为高温,故反应的化学方程式为2Mg+CO2高温 2MgO+C。通过该实验能够说明燃烧不一定需要有氧气,如镁就能在二氧化碳中的剧烈燃烧,同时也说明了二氧化碳在一定的条件下,也能支持燃烧;当然,像镁这样的活泼金属着火时,是不能用二氧化碳灭火的。故选①②③
(3)根据题意,“加热氯化铵与氢氧化钙固体混合物的方法制取氨气”,反应物的状态是固态,反应条件是加热,应选固-固加热型的发生装置A;又由于氨气密度比空气小,极易溶于水,故要用向下排空气法收集即C装置。由于氨气极易溶于水,所以当氨气溶于水后,集气瓶内压强减小,可见水面上升,而氨气的水溶液是氨水,氨水显碱性,故能使无色酚酞溶液变成红色。
考点:检查装置的气密性,常用气体的发生装置和收集装置与选取方法,实验室制二氧化碳的反应原理,二氧化碳的性质,书写化学方程式
点评:本题的重点是常用气体的发生装置和收集装置的选取方法,要学会根据反应物的状态和反应的条件选择发生装置,根据制取气体的溶解性和密度的大小选择收集气体的方法。

 金钥匙试卷系列答案
金钥匙试卷系列答案