题目内容
【题目】水是生命之源。
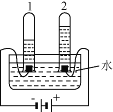
(1)电解水实验揭示了水的组成。如图实验中得到氢气的试管是_______________(填“1”或“2”)。
(2)自来水厂净水过程中用到活性炭,其作用是 。
(3)生活中常用________区分硬水和软水。
(4)海水淡化可采用膜分离技术。如图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中其他各种离子不能通过淡化膜,从而得到淡水。对加压后右侧海水成分变化分析正确的是_________。
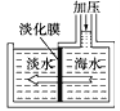
A.溶质质量增加 B.溶剂质量减少
C.溶液质量不变 D.溶质质量分数减少
【答案】(1)1 (2)吸附 (3)肥皂水 (4)B
【解析】
试题分析:(1)电解水实验揭示了水的组成。实验中得到氢气的试管为与电源负极相连的试管1;(2)自来水厂净水过程中用到活性炭,其作用是吸附;(3)生活中常用肥皂水区分硬水和软水;(4)海水淡化可采用膜分离技术。 对淡化膜一侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中其他各种离子不能通过淡化膜,从而得到淡水。对加压后右侧海水成分变化正确的是A.是错误的叙述,溶质质量不变; B.溶剂质量减少 是正确的叙述;C.是错误的叙述,溶液质量减小;D.是错误的叙述,溶质质量分数变大。

练习册系列答案
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目