题目内容
将相同体积,相同溶质质量分数的稀盐酸,分别加入到等质量、颗粒大小相同的X、Y、Z三种较活泼金属中(金属完全反应〕,生成H2的质量与反应时间的关系如下图所示.下列说法中正确的是( )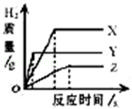
| A.消耗稀盐酸的质量顺序为Z>Y>X |
| B.产生氢气的速率顺序为X>Y>Z |
| C.三种金属的活动性顺序为Y>X>Z |
| D.相对原子质量由大到小的顺序为X>Y>Z |
C
解析试题分析:A、根据反应的原理可以知道,盐酸中的氢元素全部转化为氢气,从图表中可以看出生成氢气质量从多到少的顺序为:X、Y、Z故消耗盐酸的质量由多到少的顺序为:X>Y>Z,故A错;B、从图象中可以看出,Y反应所需时间最短,其反应速率最快,Z所需时间最长,反应最慢,故B错;C、从图象中可以看出:Y反应所需时间最短,其反应速率最快,故其活动性最强,Z所需时间最长,反应最慢,故Z的活动性最弱,故C对;D、我们知道在化合价相同的条件下,等质量的金属与足量的酸反应,相对原子质量越大,则生成气体的质量越少,但是本题中没有化合价,故难以确定其相对原子质量的大小,故D错。
考点:本题考查金属活动性顺序及其应用;根据化学反应方程式的计算。

 高效智能课时作业系列答案
高效智能课时作业系列答案下列气体中既能燃烧又能使金属氧化物还原的是
| A.氧气 | B.一氧化碳 | C.二氧化碳 | D.甲烷 |
下列关于二氧化碳的说法正确的是
| A.二氧化碳不供给呼吸,也不能作为植物养料 |
| B.实验室常用纯碱粉末和盐酸制取二氧化碳 |
| C.干冰可用作制冷剂和制造舞台云雾 |
| D.若二氧化碳在空气中含量过高,则会引发酸雨 |
向硝酸银和硝酸铜的混合溶液中加入一定量的镁粉,充分反应后再加入一定量的稀盐酸,没有气体产生,将混合液过滤,则下列说法中错误的是( )
| A.滤液中一定含有硝酸镁,可能含有硝酸铜和稀盐酸 |
| B.滤液中一定含有硝酸镁,可能含有硝酸铜和硝酸银 |
| C.滤出的固体中一定含银,可能含铜 |
| D.滤出的固体中一定含银,可能含铜和氯化银 |
某同学为探究Zn、Fe、Cu三种金属的活动性,设计了三组实验:
①将大小相同的Zn、Fe、Cu三种金属片分别插入体积和浓度均相同的稀硫酸中
②将Zn片插入硫酸铜溶液中,Cu片插入硫酸亚铁溶液中
③将Zn片插入硫酸亚铁溶液中,将Fe片插入硫酸铜溶液中
其中可以达到目的是( )
| A.①③ | B.③ | C.①② | D.②③ |
(2005?宿迁)向含AgNO3、Cu(NO3)2、Mg(NO3)2混合溶液中,加入一定量的锌粒,充分反应后过滤,向滤出的固体中滴加稀硫酸,有气体生成,则滤出的固体中一定有( )
| A.Ag、Cu、Mg | B.Cu、Mg、Zn | C.Ag、Cu、Zn | D.Ag、Mg、Zn |
向Zn(NO3)2和Cu(NO3)2 混合溶液中加入一定量的铁粉,充分反应后,过滤。向滤渣中再加入稀盐酸,有气体放出。下列说法正确的是
| A.滤渣中一定有锌 | B.滤渣中一定有铜 |
| C.所得溶液中一定有Zn2+、Cu2+ | D.所得溶液中一定有Cu2+、Fe2+ |