题目内容
(2010?达县模拟)5.6g不纯的铁片(含有下列一种金属)和足量的稀硫酸完全反应,产生氢气0.21g,则铁中含有的杂质可能是( )
【答案】分析:根据二价金属与酸反应的化学方程式来计算金属的平均式量,使平均式量介于56和另一种金属的相对原子质量之间.
解答:解:把不纯的铁看作纯二价金属M,设其相对原子质量为X,则
M+H2SO4═MSO4+H2↑
X 2
5.60g 0.21g
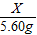 =
=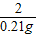
解得X═53.3
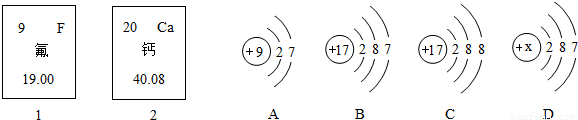
A中镁的相对原子质量为24,53.3介于24和56之间,故A正确.
B中铜不与稀硫酸反应,若含有铜时,只有铁反应,根据方程式,5.60g铁全部反应仅生成0.20g氢气,故B错误.
C中银不与稀硫酸反应,若含有银时,只有铁反应,根据方程式,5.60g铁全部反应仅生成0.20g氢气,故C错误.
D、A对故D错误.
故答案选A.
点评:本题考查了学生应用化学方程式计算判断金属的成分,注意利用平均值的方法来解答.
解答:解:把不纯的铁看作纯二价金属M,设其相对原子质量为X,则
M+H2SO4═MSO4+H2↑
X 2
5.60g 0.21g
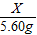 =
=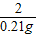
解得X═53.3
A中镁的相对原子质量为24,53.3介于24和56之间,故A正确.
B中铜不与稀硫酸反应,若含有铜时,只有铁反应,根据方程式,5.60g铁全部反应仅生成0.20g氢气,故B错误.
C中银不与稀硫酸反应,若含有银时,只有铁反应,根据方程式,5.60g铁全部反应仅生成0.20g氢气,故C错误.
D、A对故D错误.
故答案选A.
点评:本题考查了学生应用化学方程式计算判断金属的成分,注意利用平均值的方法来解答.

练习册系列答案
相关题目