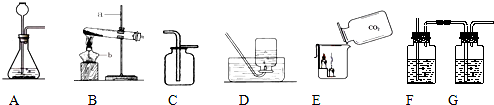
题目内容
某兴趣小组的同学在老师的指导下,对一瓶没有塞橡皮塞的氢氧化钙溶液进行探究,请你一起参与.
【提出问题】该氢氧化钙溶液是否全部变质?
【猜想与假设】猜想①:氢氧化钙溶液可能全部变质,变成碳酸钙.
猜想②:氢氧化钙溶液可能部分变质,其成分是 .
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取样于试管中,滴加稀盐酸 | 有 气泡 生成 | 原溶液里一定有碳酸钙 |
| (2)另取样于试管中,滴加酚酞试液 | 溶液成红色 | 原溶液一定有 氢氧化钙 |
【实验结论】综合上述实验(1)、(2),你得出的结论是猜想 成立.
【反思拓展】(1)氢氧化钙露置于空气中容易变质,原因是 (用化学方程式表示).
(2)在分析化学反应的物质成分时,除了考虑生成物外,还需考虑的是 反 .
| 【猜想与假设】猜想②:根据氢氧化钙变质后生成碳酸钙分析; 【实验探究】(1)根据碳酸钙能与盐酸反应生成二氧化碳气体分析; (2)根据酚酞试液遇碱变红分析; 【实验结论】根据实验(1)、(2)结论判断; 【反思拓展】(1)根据氢氧化钙和空气中的二氧化碳反应生成碳酸钙和水分析; (2)在分析化学反应的物质成分时,除了考虑生成物外,还需考虑的是反应物的量的多少; | |
| 解答: | 解:【猜想与假设】猜想②:氢氧化钙变质后,生成碳酸钙,部分变质就含有碳酸钙和氢氧化钙,故填:碳酸钙和氢氧化钙; 【实验探究】(1)碳酸钙能与盐酸反应生成二氧化碳气体,所以产生的现象为:有大量气泡产生; 故填:有大量气泡产生; (2)使酚酞试液变红的是碱性物质,所以根据混合物的组成,可以判断含有氢氧化钙,故填:氢氧化钙; 【实验结论】综合上述实验(1)、(2)可知混合物里面含有氢氧化钙和碳酸钙,所以猜想②成立,故填:②; 【反思拓展】(1)氢氧化钙露置于空气中容易变质是因为氢氧化钙和空气中的二氧化碳反应生成碳酸钙和水,反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O; (2)在分析化学反应的物质成分时,除了考虑生成物外,还需考虑的是反应物是否有剩余或反应物是否反应完全等,故填:反应物是否有剩余; |

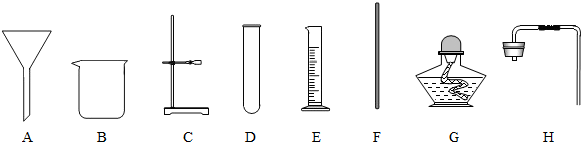
 (2011?邵阳)某化学兴趣小组的同学在老师的带领下参观如图所示的炼铁厂.小新想用自己所学知识来测定产品中铁的质量分数,征得工人师傅同意,带回一小块生铁样品.称得该样品6.0g,放入烧杯中,向其中滴加入稀盐酸,当滴入54.0g稀盐酸时,反应不再产生气泡(假设杂质不参与反应),称得烧杯内剩余物质的总质量为59.8g.(铁与稀盐酸反应的化学方程式为Fe+2HCl=FeCl2+H2↑)请你帮小新完成有关计算(结果保留一位小数):
(2011?邵阳)某化学兴趣小组的同学在老师的带领下参观如图所示的炼铁厂.小新想用自己所学知识来测定产品中铁的质量分数,征得工人师傅同意,带回一小块生铁样品.称得该样品6.0g,放入烧杯中,向其中滴加入稀盐酸,当滴入54.0g稀盐酸时,反应不再产生气泡(假设杂质不参与反应),称得烧杯内剩余物质的总质量为59.8g.(铁与稀盐酸反应的化学方程式为Fe+2HCl=FeCl2+H2↑)请你帮小新完成有关计算(结果保留一位小数):