题目内容
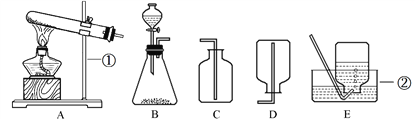
【题目】(一)小刚要模拟自来水厂的净水过程,其实验过程如下所示。请回答以下问题:

(1)A物质的名称是___________(选序号填写)。
①活性炭 ②明矾 ③石灰石 ④盐酸
(2)操作①的名称是______________, 通过操作①可除去水样中的__________(填“可溶性”或“不溶性”)杂质。在操作①中玻璃棒的作用是_________,若经过操作①后,所得液体C中仍有浑浊,其原因可能是_____________(填写序号);
a.漏斗内的滤纸有破损
b.漏斗下端未靠在烧杯内壁
c.漏斗内液面高于滤纸的边缘
(3)操作②主要是除去一些异味和色素,应选用的物质是_____________,
该过程主要是_________(填“物理”或“化学”)变化。
(4)小刚取少量液体D于试管中,加入少量肥皂水,振荡,发现有较多浮渣产生,说明液体D是______水,日常生活中常用_________ 方法使其软化后使用。
(5)中国2010上海世博会的主题是“城市,让生活更美好”。
世博园区内用“活性炭+超滤膜+紫外线”组合工艺获得直饮水。其中用紫外线代替氯气对水进行处理,其作用是________________。
(二)水是生命之源,万物之基,是人类最宝贵的自然资源。
(6)下面关于水的两个变化最本质的区别是_______________。


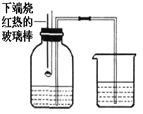
(7)右上图是水通电分解的示意图。在实验过程中,试管a中产生的气体是_________,
检验该气体的原理是_______________________(用文字表达式表示)。该过程是将电能转化为______能,通过对电解水产物的验证,说明水是由______________组成的。
(8)下图是某空间站能量转化系统局部示意图,其中水电解系统及燃料电池系统中的溶液均采用氢氧化钠溶液,下列有关说法正确的是_______。

A.该能量转化系统中的水可以循环使用
B.燃料电池系统产生的能量实际上来自于水
C.氢元素在循环过程中,没有发生化学反应
D.水电解系统中氢氧化钠溶液中的水经电解部分消耗后,氢氧化钠溶液浓度变大
【答案】 )② 过滤 不溶性 引流 a 、c 活性炭 物理 硬水 煮沸 杀菌消毒 前者是物理变化后者是化学变化 氢气 省略 化学 氢氧元素 AD
【解析】(1)明矾溶于水后生成的胶状物,能吸附水中的杂质,使浑浊的水变澄清,故选②。(2)通过过滤可除去液体中的不溶性杂质。过滤操作时,玻璃棒的作用是引流。过滤后滤液浑浊,可能的原因是漏斗内的滤纸有破损、漏斗内液面高于滤纸的边缘。(3)活性炭具有吸附性,能除去异味和色素吗,该过程无新物质生成,是物理变化。(4)硬水中加入肥皂水,出现浮渣较多。日常生活中常用煮沸的方法降低水的硬度。(5)紫外线有杀菌消毒的作用。(6)电解水是化学变化,加热水是物理变化。(7)电解水时,正氧负氢,氢二氧一。氢气+氧气![]() 水,电解水是将电能转化为化学能,通过对电解水产物的验证,说明水是由氢、氧两种元素组成的。(8)A.该能量转化系统中的水可以循环使用,正确;B.燃料电池系统产生的能量实际上来自于太阳能,错误;C.氢元素在循环过程中,发生了化学反应,错误;D.水电解系统中氢氧化钠溶液中的水经电解部分消耗后,氢氧化钠溶液浓度变大,正确。故选AD。
水,电解水是将电能转化为化学能,通过对电解水产物的验证,说明水是由氢、氧两种元素组成的。(8)A.该能量转化系统中的水可以循环使用,正确;B.燃料电池系统产生的能量实际上来自于太阳能,错误;C.氢元素在循环过程中,发生了化学反应,错误;D.水电解系统中氢氧化钠溶液中的水经电解部分消耗后,氢氧化钠溶液浓度变大,正确。故选AD。