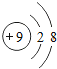题目内容
利用所学知识回答下列问题。
(1)端午节吃粽子是中华民族的传统民俗,制作原料主要有糯米、瘦肉、食盐等,其中富含蛋白质的是_________________。
(2)净化水的方法有:①过滤、②沉降、③消毒杀菌。要将混有泥沙的天然水净化成生活用的自来水,应选用的方法和顺序为____________________(填序号)。
(3)向硝酸银和硝酸铝的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入足量的稀盐酸,有气泡产生,则滤渣中一定有_________,滤液中一定有的金属离子是______(填离子符号).
在介绍氢气的制法时,老师告诉同学们,铝丝与一种可以用铁制容器盛装的溶液反应,也会生成氢气。
(提出问题)与铝丝反应的是什么溶液?
(交流讨论)分析后,大家一致认为该溶液不是稀盐酸或稀硫酸,原因是_____。
同学们决定进一步探究。老师为同学们提供了该溶液。
(查阅资料)含有不同金属离子的溶液在灼烧时会产生不同颜色的火焰
钠 | 钙 | 钾 |
黄色 | 砖红色 | 紫色(透过蓝色钴玻璃) |
(实验探究)
①小强取该溶液于试管中,向其中滴加紫色石蕊溶液,发现紫色石蕊溶液变蓝。
②小明用铂丝蘸取该溶液在酒精灯火焰上灼烧,观察到火焰呈黄色。
③有同学提出应向该溶液中滴加稀盐酸,小美取该溶液于试管中,向其中加入足量的稀盐酸后,没有看到明显现象,这样做是为了排除_____(填离子符号)的干扰。
(实验结论)该溶液为_____溶液。
(交流反思)
①老师告诉同学们,铝与该溶液反应除了生成氢气外,还生成了一种含有A1O2﹣的盐,请写出该反应的化学方程式_____。
②金属铝的化学性质较活泼,而生活中使用的铝制品却耐腐蚀,原因是_____。
某兴趣小组按照如图所示过程进行实验,实验过程中测得不同时刻装置和药品总质量随时间变化的数据见表。请计算:

时刻 | t0 | t1 | t2 | t3 | t4 |
装置和药品总质量/g | 175.0 | 243.0 | 242.4 | 241.4 | 241.4 |
(1)共制得氧气_____g。
(2)过氧化氢溶液中溶质的质量分数。_____


 取用药品 B.
取用药品 B.  滴加液体
滴加液体 加热固体药品 D.
加热固体药品 D.  量取9.5mL液体
量取9.5mL液体 B.
B. 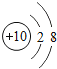 C.
C.  D.
D.