题目内容
(1)锂是一种金属单质,化学式为Li,锂原子结构示意图为 ,在反应中易
,在反应中易
(2)化学反应A→B+C,D在反应中作催化剂,12gA与3gD混合后使反应完全生成了8gB,同时生成
(3)工业酒精中常含有少量甲醇,请你根据甲醇在氧气中完全燃烧的产物是CO2和H2O推断甲醇肯定含有
 ,在反应中易
,在反应中易失去
失去
(填“失去”或“得到”) 最外层电子,则锂的氧化物的化学式为Li2O
Li2O
.(2)化学反应A→B+C,D在反应中作催化剂,12gA与3gD混合后使反应完全生成了8gB,同时生成
4
4
gC(3)工业酒精中常含有少量甲醇,请你根据甲醇在氧气中完全燃烧的产物是CO2和H2O推断甲醇肯定含有
碳、氢
碳、氢
元素.分析:(1)很据元素的性质与最外层电子数的关系分析,根据化合价写出化学式;
(2)根据质量守恒定律分析判断;
(3)根据质量守恒定律反应前后元素的种类不变分析.
(2)根据质量守恒定律分析判断;
(3)根据质量守恒定律反应前后元素的种类不变分析.
解答:解:(1)由锂原子结构示意图可知,最外层电子数是1,少于4个,在反应中易失去1个电子.,锂元素化合价为+1价,氧元素的化合价为-2价,形成的氧化物的化学式是:Li2O.
(2)由题意可知,在化学反应A→B+C,D在反应中作催化剂,12gA与3gD混合后使反应完全生成了8gB,根据质量守恒定律可知,生成的C的质量为:12g-8g=4g.
(3)甲醇在氧气中完全燃烧的产物是CO2和H2O,由于生成物种含有碳、氢、氧三种元素,由质量守恒定律反应前后元素的种类不变可知.则甲醇肯定含有碳、氢元素,可能含有氧元素.
故答为:(1)失去;Li2O.(2)4;(3)碳、氢.
(2)由题意可知,在化学反应A→B+C,D在反应中作催化剂,12gA与3gD混合后使反应完全生成了8gB,根据质量守恒定律可知,生成的C的质量为:12g-8g=4g.
(3)甲醇在氧气中完全燃烧的产物是CO2和H2O,由于生成物种含有碳、氢、氧三种元素,由质量守恒定律反应前后元素的种类不变可知.则甲醇肯定含有碳、氢元素,可能含有氧元素.
故答为:(1)失去;Li2O.(2)4;(3)碳、氢.
点评:准确理解质量真守恒定律,会应用判断物质的质量或组成元素等.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
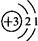 ,易失去最外层一个电子.则锂的氧化物的化学式为
,易失去最外层一个电子.则锂的氧化物的化学式为 ,易失去最外层一个电子.则锂的氧化物的化学式为
,易失去最外层一个电子.则锂的氧化物的化学式为
 易失去最外层一个电子.则锂的氧化物的化学式为
易失去最外层一个电子.则锂的氧化物的化学式为 ,易失去最外层一个电子.则锂的氧化物的化学式为______.
,易失去最外层一个电子.则锂的氧化物的化学式为______.