题目内容
【题目】氯化钙在生活中常用作干燥剂、融雪剂,在工业上可用于制造防冻液等.某工厂以石灰石为原料生产二水氯化钙(CaCl22H2O)的流程如图.原料石灰石中含有杂质主要是MgCO3、MgSO4和Al2O3.
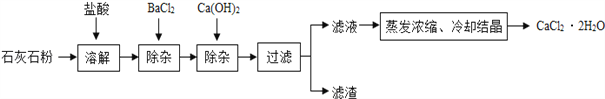
(1)过滤操作用到的玻璃仪器之一为_________________.
(2)石灰石粉溶解时,Al2O3发生反应的化学方程式为_____.
(3)加入BaCl2除去的杂质离子是____;加入Ca(OH)2除去的杂质离子是__.
(4)检验“滤液”酸碱性,如果显碱性,还需加入适量的___(填化学式)提高产品纯度.
【答案】 漏斗 Al2O3 + 6HCl = 2AlCl3 + 3H2O 硫酸根离子 镁离子和铝离子 HCl
【解析】(1)过滤操作需要的玻璃仪器有三角漏斗、玻璃棒及烧杯;
(2)氧化铝与盐酸反应生成氯化铝和水,化学方程式为Al2O3+6HCl=2AlCl3+3H2O;
(3)氯化钡能与溶液中的硫酸镁反应生成硫酸钡沉淀和氯化镁,因此,除去的杂质离子为硫酸根离子;氢氧化钙能与溶液中氯化镁、氯化铝反应生成氢氧化镁沉淀、氢氧化铝沉淀和氯化钙,因此,除去的杂质离子为镁离子、铝离子;
(4)如果滤液显碱性,则前后操作中加入的氢氧化钙过量,可加入稀盐酸与氢氧化钙反应生成氯化钙和水,除去氢氧化钙而得到较为纯净的氯化钙.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目