题目内容
【题目】氧化镁、氧化铜、氧化铁组成的混合物 28 克,与 500 克质量分数为 9.8%稀硫酸恰好完全反应,再向所得溶液中加入 600 克溶质质量分数为 10%的氢氧化钠溶液,充分反应后,过滤,干燥得到的固体质量为( )
A.37gB.38.5gC.41.5gD.53.5g
【答案】A
【解析】
氧化镁、氧化铜、氧化铁与硫酸反应生成硫酸镁、硫酸铜、硫酸铁,然后硫酸镁、硫酸铜、硫酸铁与氢氧化钠反应生成氢氧化镁、氢氧化铜、氢氧化铁,此题可以根据质量守恒定律,先判断硫酸与氢氧化钠是否完全反应,从而得出固体的质量就是原混合物中金属的质量与参加反应氢氧化钠中氢氧根的质量和。
设与 500 克质量分数为 9.8%稀硫酸反应的氢氧化钠的质量为x,
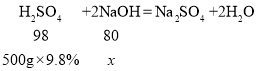
![]()
x=40g,
600 克溶质质量分数为 10%的氢氧化钠溶液中氢氧化钠的质量600 克![]() 10%=60克,所以氢氧化钠剩余;氧化镁、氧化铜、氧化铁与硫酸反应生成硫酸镁、硫酸铜、硫酸铁和水,所以生成水中氧元素的质量等于氧化镁、氧化铜、氧化铁中氧元素的质量,设水中氧元素的质量为y,则:
10%=60克,所以氢氧化钠剩余;氧化镁、氧化铜、氧化铁与硫酸反应生成硫酸镁、硫酸铜、硫酸铁和水,所以生成水中氧元素的质量等于氧化镁、氧化铜、氧化铁中氧元素的质量,设水中氧元素的质量为y,则:
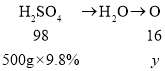
![]()
y=8g,
得到的固体质量=28g-8g+40g![]()
![]() =37g。
=37g。
故选A。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目