题目内容
【题目】为了测定某赤铁矿石中氧化铁(Fe2O3)的质量分数,取矿石样品20克,加入稀盐酸,恰好完全反应时,共消耗稀盐酸219克,经过过滤、洗涤、干燥后得到滤渣4克(注:矿石中的杂质既不溶于水,也不与盐酸反应)。请计算:
(1)赤铁矿石含氧化铁的质量;(2)稀盐酸的溶质质量分数。
【答案】(1)16g -(2)10%
【解析】
试题分析:(1)根据题意,氧化铁与盐酸恰好完全反应,而矿石中的杂质既不溶于水也不盐酸反应,即反应之后得到的滤渣是杂质,故赤铁矿石中氧化铁的质量为:20g-4g=16g
(2)解:设稀盐酸的溶质质量分数为x
Fe2O3+6HCl![]() 2FeCl3+3H2O
2FeCl3+3H2O
160 6×36.5
16g 219g.x
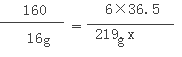
X=10%
答:稀盐酸的溶质质量分数为10%

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目

