题目内容
(7分)
某化学兴趣小组同学欲除去固体氯化钠中混有的氯化钙。设计实验方案如下,请参与实验并回答问题。

⑴写出A物质的化学式: ,写出A物质的俗称: 。
⑵写出反应②的化学方程式: 。
⑶反应①中加入过量A物质的目的是 ;反应②中如果加入盐酸也过量,则对所得到的氯化钠纯度 (填“有”或“没有”)影响。
⑷分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果
(填“增大”、“不变”或“减少”)
某化学兴趣小组同学欲除去固体氯化钠中混有的氯化钙。设计实验方案如下,请参与实验并回答问题。

⑴写出A物质的化学式: ,写出A物质的俗称: 。
⑵写出反应②的化学方程式: 。
⑶反应①中加入过量A物质的目的是 ;反应②中如果加入盐酸也过量,则对所得到的氯化钠纯度 (填“有”或“没有”)影响。
⑷分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果
(填“增大”、“不变”或“减少”)
⑴Na2CO3;纯碱。
⑵Na2CO3+2HCl=2NaCl+H2O+CO2↑;
⑶使氯化钙完全反应(合理即可);没有
⑷增大。
⑵Na2CO3+2HCl=2NaCl+H2O+CO2↑;
⑶使氯化钙完全反应(合理即可);没有
⑷增大。
分析:本题中的氯化钠和氯化钙都属于盐,属于除杂质题,除杂质题最少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应②反应时不能加入新的杂质.要除去氯化钠中的少量杂质氯化钙,只要除去钙离子就可以了,氯离子不是杂质.因此可以加入足量是碳酸钠溶液(俗名纯碱或苏打),生成白色沉淀碳酸钙,从而除去钙离子,得到的沉淀和溶液可以用过滤的方法分开.过量的碳酸钠可以用稀盐酸除去,在每个步骤中都有氯化钠生成,因此氯化钠的质量是增加的.
解答:解:(1)要除去氯化钠中的少量杂质氯化钙,只要除去钙离子就可以了,氯离子不是杂质.因此可以加入足量是碳酸钠溶液,生成白色沉淀碳酸钙,从而除去钙离子.碳酸钠的俗名是纯碱或苏打.故答案为:Na2CO3;纯碱(或苏打).
(2)②的化学方程式是指过量的碳酸钠与稀盐酸的反应,它们互相交换成分生成氯化钠和水和二氧化碳,要注意配平.故答案为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(3)反应①中加入过量A物质的目的是使氯化钙充分反应;反应②中如果加入盐酸也过量,对所得的氯化钠的纯度无影响,因为盐酸具有挥发性并且是液体.故答案为:使氯化钙完全反应(合理即可);没有.
(4)分离后所得氯化钠的质量与原来氯化钠的质量相比较增多了,原因是每一步除杂质的过程中都生成了氯化钠.故答案为:增大.
解答:解:(1)要除去氯化钠中的少量杂质氯化钙,只要除去钙离子就可以了,氯离子不是杂质.因此可以加入足量是碳酸钠溶液,生成白色沉淀碳酸钙,从而除去钙离子.碳酸钠的俗名是纯碱或苏打.故答案为:Na2CO3;纯碱(或苏打).
(2)②的化学方程式是指过量的碳酸钠与稀盐酸的反应,它们互相交换成分生成氯化钠和水和二氧化碳,要注意配平.故答案为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(3)反应①中加入过量A物质的目的是使氯化钙充分反应;反应②中如果加入盐酸也过量,对所得的氯化钠的纯度无影响,因为盐酸具有挥发性并且是液体.故答案为:使氯化钙完全反应(合理即可);没有.
(4)分离后所得氯化钠的质量与原来氯化钠的质量相比较增多了,原因是每一步除杂质的过程中都生成了氯化钠.故答案为:增大.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目





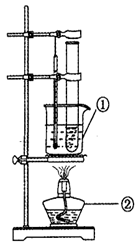



 ③ 设计“实验1”的目的是 。
③ 设计“实验1”的目的是 。 (I) 2KClO3 + 2MnO2="==2KMnO4" + Cl2↑+ O2↑;
(I) 2KClO3 + 2MnO2="==2KMnO4" + Cl2↑+ O2↑; (III)K2MnO4 + Cl2="==2KCl" + MnO2 + O2↑。
(III)K2MnO4 + Cl2="==2KCl" + MnO2 + O2↑。