题目内容
【题目】结合下图回答问题:
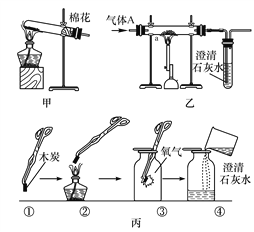
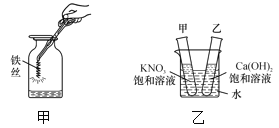
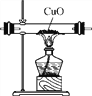
(1)实验室用甲装置制取氧气,该反应的化学方程式为___________________________________。
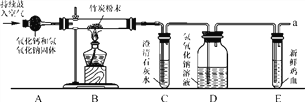
(2)若工业上使用赤铁矿石(主要成分是氧化铁)炼铁,请写出炼铁原理的化学方程式:________________________。在实验室里,可以利用乙装置进行此实验,点燃酒精喷灯前先通一会儿气体A的目的是__________________________________________________________。
(3)丙实验是验证木炭具有在氧气中能燃烧的性质实验,第④步操作中,应待瓶内温度___________时,再倒入澄清石灰水、振荡。其中第④步的实验目的是________________________________。
【答案】 2KMnO4![]() K2MnO4+MnO2+O2↑ Fe2O3+3CO
K2MnO4+MnO2+O2↑ Fe2O3+3CO![]() 2Fe+3CO2 排尽装置内的空气,防止加热时发生爆炸 恢复到室温 检验木炭在氧气中燃烧的产物是二氧化碳
2Fe+3CO2 排尽装置内的空气,防止加热时发生爆炸 恢复到室温 检验木炭在氧气中燃烧的产物是二氧化碳
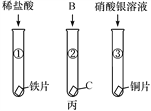
【解析】(1)如图所示实验装置属于固体加热型制取气体,且试管口有一团棉花,故是采用了加热高锰酸钾的方法制取氧气;高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,反应的化学方程式是2KMnO4![]() K2MnO4+MnO2+O2↑;(2)炼铁的原理是一氧化碳还原氧化铁,其方程式是:可燃性气体在点燃或加热前一定要验纯,如果可燃性气体中混有空气(氧气)点燃时会发生爆炸,所以通一氧化碳排尽试管内的空气,防止试管里的空气与一氧化碳混合反应而发生爆炸; (3)通过①铁能与稀盐酸反应,说明铁的金属活动性比氢强;②中铁能与硫酸铜反应,说明铁的金属活动性比铜强,即Fe>Cu;③中铜能与硝酸银溶液反应,说明铜的金属活动性比银强,即Cu>Ag;④铜不能与稀盐酸反应,说明铜的金属活动性比氢弱.由上述分析可知,能验证Fe、Cu、Ag三种金属的活动性顺序的实验方案中,需要最少的实验组合是②③,即B正确。
K2MnO4+MnO2+O2↑;(2)炼铁的原理是一氧化碳还原氧化铁,其方程式是:可燃性气体在点燃或加热前一定要验纯,如果可燃性气体中混有空气(氧气)点燃时会发生爆炸,所以通一氧化碳排尽试管内的空气,防止试管里的空气与一氧化碳混合反应而发生爆炸; (3)通过①铁能与稀盐酸反应,说明铁的金属活动性比氢强;②中铁能与硫酸铜反应,说明铁的金属活动性比铜强,即Fe>Cu;③中铜能与硝酸银溶液反应,说明铜的金属活动性比银强,即Cu>Ag;④铜不能与稀盐酸反应,说明铜的金属活动性比氢弱.由上述分析可知,能验证Fe、Cu、Ag三种金属的活动性顺序的实验方案中,需要最少的实验组合是②③,即B正确。