题目内容
【题目】已知碳12原子的质量为1.993×10﹣26kg,若A 原子的质量为9.288×10﹣26kg,且A原子核内质子数比中子数少4个.试计算:
(1)A原子的相对原子质量是多少?(结果为整数)
(2)A原子的核外电子数是多少?
(3)A原子的中子数是多少?
【答案】
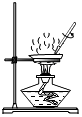
(1)解:碳12原子的质量为1.993×10﹣26kg,若A 原子的质量为9.288×10﹣26kg,A原子的相对原子质量是 ![]() ≈56
≈56
(2)解:相对原子质量=质子数+中子数,A原子核内质子数比中子数少4个,设质子数为x,则x+x+4=56,x=26;原子中:核电荷数=核内质子数=核外电子数,则A原子的核外电子数是26
(3)解:A原子核内质子数比中子数少4个,则A原子的中子数是26+4=30
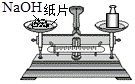
【解析】(1)根据某原子的相对原子质量= ![]() ,结合题意进行分析解答即可.(2)根据原子中:核电荷数=核内质子数=核外电子数,相对原子质量=质子数+中子数,进行分析解答.(3)根据A原子核内质子数比中子数少4个,进行分析解答.
,结合题意进行分析解答即可.(2)根据原子中:核电荷数=核内质子数=核外电子数,相对原子质量=质子数+中子数,进行分析解答.(3)根据A原子核内质子数比中子数少4个,进行分析解答.

练习册系列答案
相关题目