题目内容
【题目】某化学课堂将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
(演示实验)将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
(学生板演)该反应的化学方程式_____.
(提出问题)实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
(假设猜想)针对疑问,太家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4
猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH
猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是_____.
(实验探究)
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有_____.
(2)老师给小组提供了pH试纸、铜片、BaCl2溶液、Na2CO3溶液,请设计2个方案继续按如表探究.
实验操作 | 预期现象及结论 |
_____ | _____ |
____ | ____ |
【答案】![]() 四 NaOH或氢氧化钠 取少量待测溶液,滴加碳酸钠溶液 若有气泡产生,则猜想二正确;否则猜想一正确 用玻璃棒蘸取少量溶液涂到pH试纸上,观察颜色的变化,然后与标准比色卡对照,测出溶液的pH值 pH<7,则猜想二正确;pH=7,则猜想一正确
四 NaOH或氢氧化钠 取少量待测溶液,滴加碳酸钠溶液 若有气泡产生,则猜想二正确;否则猜想一正确 用玻璃棒蘸取少量溶液涂到pH试纸上,观察颜色的变化,然后与标准比色卡对照,测出溶液的pH值 pH<7,则猜想二正确;pH=7,则猜想一正确
【解析】
学生板演:硫酸和氢氧化钠反应生成硫酸钠和水,该反应的化学方程式为![]() ;故填:
;故填:![]() ;
;
假设猜想:硫酸和氢氧化钠反应生成硫酸钠和水,酸或碱可能过量,但不能同时过量,因为酸碱不能共存,会继续反应,故猜想四不合理;故填:四;
实验探究:(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有NaOH或氢氧化钠,因为氢氧化钠能与硫酸铜反应生成氢氧化铜和硫酸钠,故填:NaOH或氢氧化钠;
(2)由(1)得出,溶液中一定没有氢氧化钠,故现在只需验证溶液中是否含硫酸,碳酸钠和硫酸反应能生成二氧化碳气体,故可用碳酸钠验证是否含硫酸,实验操作:取少量待测溶液,滴加碳酸钠溶液;预期现象及结论:若有气泡产生,则猜想二正确;否则猜想一正确;
硫酸显酸性,pH<7,硫酸钠显中性,pH=7,故可用pH试纸来验证,实验操作:用玻璃棒蘸取少量溶液涂到pH试纸上,观察颜色的变化,然后与标准比色卡对照,测出溶液的pH值;预期现象及结论:pH<7,则猜想二正确;pH=7,则猜想一正确。

 一线名师权威作业本系列答案
一线名师权威作业本系列答案【题目】某同学在学习溶液时进行了如下实验探究:
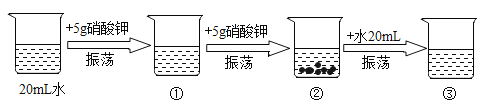
(1)上述实验所形成的溶液中,溶质是____.
(2)上述①②③烧杯的溶液,一定属于饱和溶液的是____[填烧杯编号].
(3)若要使烧杯②中的剩余固体全部溶解,除了实验中已经采取的措施外,还可以采取的措施为:____.
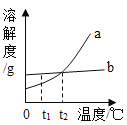
(4)图是氯化钠和硝酸钾两种固体物质的溶解度曲线,图中b表示的____溶解度曲线;在t1℃时,硝酸钾饱和溶液中溶质的质量分数____(填大于、小于或等于)氯化钠饱和溶液中溶质的质量分数.氯化钠和硝酸钾两种物质的溶解度随温度(0~100℃)的变化见下表:
0℃ | 20℃ | 40℃ | 60℃ | 80℃ | 100℃ | |
NaCl(g) | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
KNO3(g) | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |