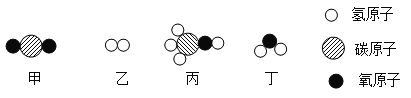
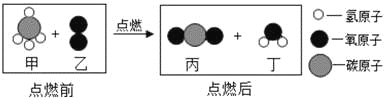
��Ŀ����
����Ŀ��С������ijʳƷ��װ������һ��С��������������ɷ֣���ʯ�ҡ����ۣ����ã����������������������������˴��ڽ��ĩ�Ƿ���ʧЧ��ȡ������ĩ��ˮ�г���ܽ⣬������ɫ��̪���ֲ���ɫ��ͨ���������ϻ�֪�����������ڿ����в��ܷ�Ӧ����Fe3O4��FeO�����ǶԷ�ĩ�ɷ��������²��룺
����һ��������CaCO3��Fe��
�������������CaCO3��Fe2O3��
��������������_____��
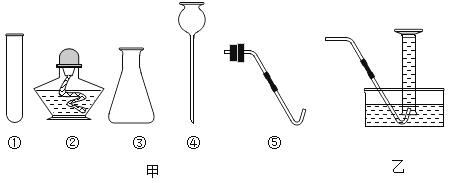
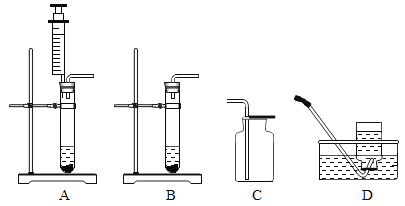
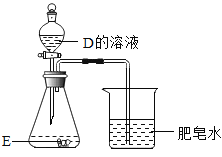
��ʵ����ƣ�С���������ͼ��ʾ��ʵ�飺

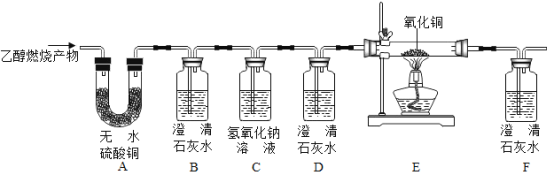
��ʵ���������
��1����Aװ���м���ϡ���ᣬBװ���г��ֻ�������֤����Ʒ�к���CaCO3��
��2������ĩ�к���Fe��װ��E��Ӧ�۲쵽��������_____��
�������뷴˼��
����ʵ���У������Eװ��ȥ�����Ƿ�����֤��ĩ�к���Fe����˵������_____��
���𰸡�CaCO3��Fe��Fe2O3 ��ˮ����ͭ����ɫ �ܣ���ͨ��D������ͭ����ɫ�仯���ж�
��������
�����������������ߵĻ���������CaCO3��Fe��Fe2O3�����CaCO3��Fe��Fe2O3��
[ʵ�������]��2������ĩ�к���Fe��������ϡ���ᷴӦ����������������������ͭ��Ӧ����ͭ��ˮ��������ˮ����ͭ��ˮ����ɫ�����۲쵽��ˮ����ͭ��ˮ����ɫ�������ˮ����ͭ����ɫ��
[�����뷴˼]�������л�ԭ�ԣ��ڼ�����������������ͭ��Ӧ����ͭ��ˮ��D�л�۲쵽��ɫ��ĩ��졣����ܣ���ͨ��D������ͭ����ɫ�仯���жϡ�

 �ִʾ�ƪ��ͬ�����Ĵ��ϵ�д�
�ִʾ�ƪ��ͬ�����Ĵ��ϵ�д� �߽�������ϵ�д�
�߽�������ϵ�д�����Ŀ��ѧϰ�˶������̶Թ�������ֽ��д����õ�֪ʶ��ijͬѧ�룺����ͭ�ܷ������ƶ������̵Ĵ������أ����Ǹ�ͬѧ����������̽����
�����룩
I������ͭ���Ǵ�����Ҳ�����뷴Ӧ����Ӧǰ�������ͻ�ѧ���ʲ��䣻
������ͭ���뷴Ӧ������������Ӧǰ�������ͻ�ѧ���ʷ����˱仯��
������ͭ�Ƿ�Ӧ�Ĵ�������Ӧǰ��_____________��
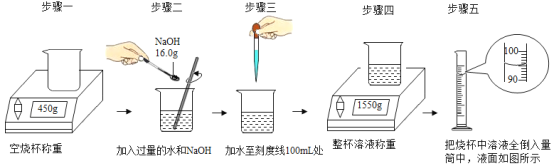
��ʵ�飩����ƽ����0.2g����ͭ��ȡ5m5%�Ĺ���������Һ���Թ��У���������ʵ�飺
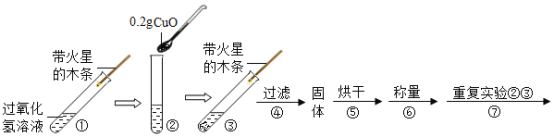
��1��������У�����ͭ�Ƿ�Ӧ�Ĵ�������Ӧǰ��________��
��2��������
��������� | ������ | ��������� | ���� |
__________�������ǵ�ľ����ȼ | __________ | ��Һ�������ݷų� | ����I���������������� |
��3������ٵ�Ŀ����_______________��
��4������ߵ�Ŀ����____________��
��5�����������ܱ�����ͭ���ֽ�ų����������ֱ���ʽΪ__________