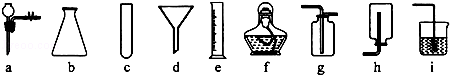题目内容
甲、乙、丙三位同学在活动课上探究气体的制备.利用下图所示装置制取常见的气体,并对它们的有关性质进行研究,请根据题意回答下列问题.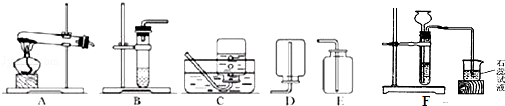
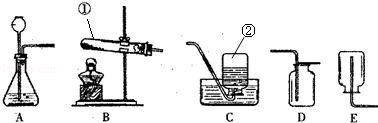
(1)甲同学用KMnO4固体制取O2,发生装置应选用上图中的 装置(填编号),该反应的化学方程式为 ;当O2收集满并取出集气瓶后,停止该实验的正确操作方法是
(2)乙同学用浓盐酸与大理石在F装置中反应,制取CO2并检验其有关性质,观察到烧杯中紫色石蕊试液变红,对这一现象的解释不合理是 (填序号).
a.产生的CO2直接使石蕊变红
b.产生的CO2与H2O反应生成H2CO3,使石蕊试液变红
c.挥发出的氯化氢溶于水,使石蕊试液变红
(3)丙同学在实验室氯化铵固体与碱石灰固体共热来制取氨气(NH3).常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水。
①制取氨气反应的化学方程式:2NH4Cl+Ca(OH)2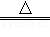 CaCl2+2NH3↑+2X.X的化学式为: .
CaCl2+2NH3↑+2X.X的化学式为: .
②制取并收集NH3,应该从上图中选择的收集装置是 .
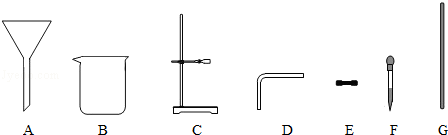
③NH3是一种碱性气体,干燥时不能选用下列干燥剂中的 .(填序号).
A.固体氢氧化钠 B.浓硫酸 C.生石灰.
(1)A;2KMnO4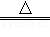 K2MnO4+MnO2+O2↑;先把导气管移出水面,再熄灭酒精灯
K2MnO4+MnO2+O2↑;先把导气管移出水面,再熄灭酒精灯
(2)a
(3)①H2O;②D;③B
解析试题分析:
(1)用KMnO4固体制取O2,是固体的加热反应,所以我们可以用装置A作为实验装置;根据反应物是高锰酸钾、反应条件是加热写出化学反应式是:2KMnO4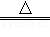 K2MnO4+MnO2+O2↑;实验结束时,为防止水倒流入试管,引起试管炸裂,要先移出导管,再熄灭酒精灯.
K2MnO4+MnO2+O2↑;实验结束时,为防止水倒流入试管,引起试管炸裂,要先移出导管,再熄灭酒精灯.
(2)从图示可知,F装置的烧杯中盛放的是石蕊试液,它遇酸变红.二氧化碳不能直接使石蕊试液变红,所以a不合理;产生的CO2与H2O反应生成H2CO3,使紫色石蕊试液变红,是正确的;挥发出的氯化氢溶于水,使溶液呈酸性,使紫色石蕊试液变红,是正确的.
(3)实验室常用氯化铵固体与碱石灰固体共热来制取氨气,①制取氨气反应的方程式:2NH4Cl+Ca(OH)2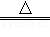 CaCl2+2NH3↑+2X.X的化学式为:H2O;②收集NH3应该从上图中选择的收集装置是D,因为它密度比空气小,极易溶于水.③A和C都显碱性,可用来干燥氨气,B显酸性,会与氨气发生反应,不能用来干燥氨气
CaCl2+2NH3↑+2X.X的化学式为:H2O;②收集NH3应该从上图中选择的收集装置是D,因为它密度比空气小,极易溶于水.③A和C都显碱性,可用来干燥氨气,B显酸性,会与氨气发生反应,不能用来干燥氨气
考点:常用气体的发生装置和收集装置与选取方法;实验室制取氧气的反应原理;制取氧气的操作步骤和注意点;二氧化碳的实验室制法;酸的物理性质及用途;根据浓硫酸或烧碱的性质确定所能干燥的气体;质量守恒定律及其应用


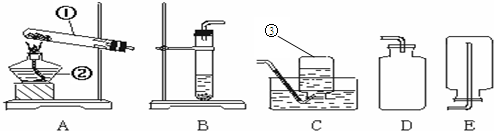
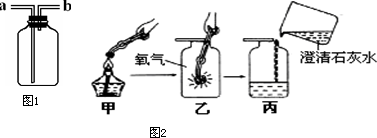








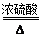 CO↑+CO2↑+H2O,已知CO气体密度与空气接近,难溶于水,实验室收集CO气体的装置是 (填字母),为了收集到纯净的CO气体,必须利用图1的装置甲除去CO2,装置乙除去水蒸气,则装置甲应盛放 (填序号,下同),乙应盛放 。
CO↑+CO2↑+H2O,已知CO气体密度与空气接近,难溶于水,实验室收集CO气体的装置是 (填字母),为了收集到纯净的CO气体,必须利用图1的装置甲除去CO2,装置乙除去水蒸气,则装置甲应盛放 (填序号,下同),乙应盛放 。