题目内容
实验室用200g某浓度的氢氧化钠溶液充分吸收二氧化硫,如共吸收了0.3mol的二氧化硫,假设恰好完全反应.
(1)该氢氧化钠溶液中氢氧化钠的物质的量是多少?(根据化学方程式列式计算)
(2)上述氢氧化钠溶液的溶质质量分数为________.
解:(1)设该氢氧化钠溶液中氢氧化钠的物质的量是x,
2NaOH+SO2═Na2SO3+H2O
2 1
x 0.3mol
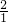 =
=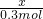
x=0.6mol;
答:该氢氧化钠溶液中氢氧化钠的物质的量是0.6mol;
(2)0.6mol氢氧化钠的质量为0.6mol×40g/mol=24g.
氢氧化钠溶液的溶质质量分数为: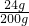 ×100%=12.0%.
×100%=12.0%.
故答案为:12.0%.
分析:(1)根据氢氧化钠与二氧化硫反应的化学方程式和二氧化硫的质量,列出比例式,就可计算出该氢氧化钠溶液中氢氧化钠的物质的量;
(2)根据溶质质量分数=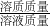 ×100%计算即可.
×100%计算即可.
点评:本题主要考查学生利用化学方程式和溶质质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.
2NaOH+SO2═Na2SO3+H2O
2 1
x 0.3mol
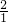 =
=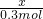
x=0.6mol;
答:该氢氧化钠溶液中氢氧化钠的物质的量是0.6mol;
(2)0.6mol氢氧化钠的质量为0.6mol×40g/mol=24g.
氢氧化钠溶液的溶质质量分数为:
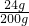 ×100%=12.0%.
×100%=12.0%.故答案为:12.0%.
分析:(1)根据氢氧化钠与二氧化硫反应的化学方程式和二氧化硫的质量,列出比例式,就可计算出该氢氧化钠溶液中氢氧化钠的物质的量;
(2)根据溶质质量分数=
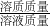 ×100%计算即可.
×100%计算即可.点评:本题主要考查学生利用化学方程式和溶质质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目