题目内容
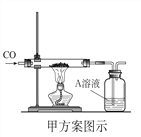
【题目】(发现问题)如图,某化学兴趣小组在用盐酸和大理石制得的二氧化碳通入澄清的石灰水时,发现澄清的石灰水并没有变浑浊。
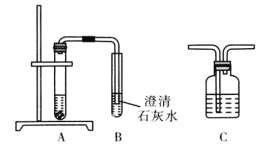
(提出问题)澄清的石灰水为什么不变浑浊呢?
(作出假设)
猜想(1):可能是澄清的石灰水时间长变质了。请写出支持他这种想法的理由:_____(用化学方程式表示)。
猜想(2):可能所用的盐酸浓度大了。请写出支持他这种想法的理由:_____。
猜想(3):有可能是盐酸浓度大,同时澄清石灰水也变质了。
(设计与实验)小芳将B中澄清的石灰水换成新制的,结果发现澄清石灰水还是不浑浊,说明猜想(1)______;
小光将A中换成溶质质量分数为5%的盐酸,结果发现澄清石灰水变浑浊了,说明猜想(2)______;
小洁在试管A、B之间连接进洗气瓶C,C中盛放的仍然是原来的澄清石灰水,结果发现B中的澄清石灰水变浑浊了,她得出了与小光同样的结论,则C中的现象为____。
(反思与提高)小洁利用一个洗气瓶C,就能使B中的澄清石灰水出现了浑浊现象,你能否将C中的澄清石灰水换成其他物质,也使B中的澄清石灰水变浑浊。请举出两种物质名称并简要说明理由。
C中可用物质 | 简明理由 |
__________ | ________ |
__________ | ________ |
【答案】CO2+Ca(OH)2=CaCO3↓+H2O 挥发出来的氯化氢气体溶于氢氧化钙溶液并与其反应,从而使二氧化碳不能与氢氧化钙反应产生沉淀 不正确 正确 C中产生气泡,但是无其他明显现象 碳酸氢钠溶液 碳酸氢钠溶液能与盐酸反应而不与二氧化碳反应 水 因为氯化氢气体极易溶于水,而二氧化碳能溶于水(溶解度较小)
【解析】
[作出假设](1)氢氧化钙会吸收空气中的二氧化碳生成碳酸钙白色沉淀和水;化学方程式:CO2+Ca(OH)2=CaCO3↓+H2O;
(2)浓盐酸具有挥发性,挥发出来的氯化氢气体溶于氢氧化钙溶液并与其反应,从而使二氧化碳不能与氢氧化钙反应产生沉淀;
[设计与实验]小芳将B中澄清的石灰水换成新制的,结果发现澄清石灰水还是不浑浊,说明石灰水并没有变质,即猜想(1)不正确;
小光将A中换成溶质质量分数为5%的盐酸,结果发现澄清石灰水变浑浊了,证明这是由于所用的盐酸浓度大造成的,即猜想(2)正确;
若小光的结论正确,即盐酸的浓度大,C中盛放的仍然是原来的澄清石灰水,那么氯化氢气体溶于水形成盐酸,盐酸与氢氧化钙反应生成氯化钙和水,发现C中产生气泡,但是无其他明显现象;
[反思与提高]洗气瓶C中可装入碳酸氢钠溶液,二氧化碳中混有的氯化氢溶于水形成盐酸,碳酸氢钠与盐酸反应生成氯化钠、水和二氧化碳,而二氧化碳与碳酸氢钠不反应,从而将氯化氢气体除去;
还可以在洗气瓶C内装入水,因为氯化氢气体极易溶于水,而二氧化碳能溶于水(溶解度较小),从而将二氧化碳中混有的氯化氢气体除去。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某校兴趣小组在实验室中完成制取氧气的实验。他们取氯酸钾和二氧化锰的混合物共3.0g放入大试管中加热,并在不同时刻测定试管内剩余固体物质的质量(如表):
分析表中数据,完成下列问题:
反应时间/min | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
剩余固体质量/g | 2.55 | 2.25 | 2.10 | 2.04 | 2.04 |
(1)加热到_____min,氯酸钾已经完全分解;
(2)完全反应后,生成氧气的质量为_____g;
(3)原混合物中氯酸钾的质量是多少_____?