题目内容
【题目】根据下图回答有关问题: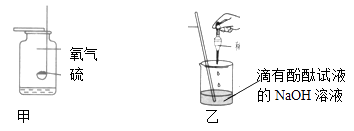
(1)甲实验中,硫在氧气中燃烧比在空气中燃烧更剧烈,说明物质反应的剧烈程度与有关。
(2)乙实验中,向烧杯中滴入盐酸至过量,发生反应的化学方程式是。以下证明盐酸过量的操作及对现象的叙述正确的是(填序号)。
A.加入蒸馏水,搅拌后溶液颜色不变 B.另加入NaOH溶液,搅拌后溶液颜色不变
C.加入AgNO3溶液,有白色沉淀产生 D.加入铁粉,有气泡产生
【答案】
(1)反应物的浓度
(2)NaOH+HCl=NaCl+H2O,BD
【解析】(1)实验的差别是氧气的含量,即说明物质反应的剧烈程度与反应物的浓度有关。(2)发生了酸碱中和反应即NaOH+HCl=NaCl+H2O;如果酸过量可以另加入NaOH溶液,搅拌后溶液颜色不变或加入铁粉,有气泡产生即BD。
所以答案是:反应物的浓度、NaOH+HCl=NaCl+H2O、BD。
【考点精析】本题主要考查了燃烧与燃烧的条件的相关知识点,需要掌握燃烧的条件:(缺一不可)(1)可燃物(2)氧气(或空气)(3)温度达到着火点才能正确解答此题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】下图是元素周期表的一部分。这四种元素均位于第_____周期,原子序数为12的元素名称为_____;玻璃的主要成分SiO2能与氢氟酸(HF)发生反应生成SiF4气体和水,反应的化学方程式为:_____。
11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 |



