题目内容
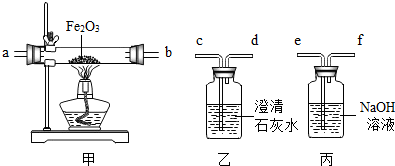
 某化学兴趣小组想探究爆炸现场附近的空气中是否含有CO气体.设计实验方案如下:
某化学兴趣小组想探究爆炸现场附近的空气中是否含有CO气体.设计实验方案如下:确定气体样品中是否含有CO.
①除去收集的空气样品中的氧气;②3CO+Fe2O3
| ||
请根据他们的设计回答下列问题:
(1)在实验时,上述仪器的连接顺序是:丙→乙→甲→乙.其中乙装置需要使用两次,第一次的作用是
检验原气体样品中的二氧化碳是否除尽
检验原气体样品中的二氧化碳是否除尽
(2)根据实验中出现的
甲中药品由红变黑
甲中药品由红变黑
或乙中石灰水第一次不变浑浊,第二次变浑浊
乙中石灰水第一次不变浑浊,第二次变浑浊
现象,能判断出爆炸现场附近的空气样品中有较多CO.(3)从环境保护的角度考虑,你认为该实验的设计是否存在缺陷,如果有,该如何改进?
有缺陷,在d处将尾气点燃(或在d处用气球收集尾气等其它合理答案也可)
有缺陷,在d处将尾气点燃(或在d处用气球收集尾气等其它合理答案也可)
.分析:氢氧化钠溶液能够吸收二氧化碳气体,二氧化碳能使澄清的石灰水变浑浊;一氧化碳有毒,能够污染环境.
解答:解:(1)因为空气中的二氧化碳对实验有干扰作用,应该除去,用氢氧化钠溶液吸收二氧化碳,用澄清的石灰水可以检验空气中的二氧化碳是否除尽.用甲装置一氧化碳还原氧化铁,通过澄清石灰水验证生成物中是否有二氧化碳,第一次乙装置的作用是检验原气体样品中的二氧化碳是否除尽;
(2)如果有一氧化碳,则一氧化碳能和氧化铁反应生成黑色的铁粉和二氧化碳,二氧化碳能使澄清的石灰水变浑浊.所以实验现象:甲中药品由红变黑或乙中石灰水第一次不变浑浊,第二次变浑浊,可以说明含有较多的一氧化碳;
(3)一氧化碳有毒,能够污染环境,要对尾气进行处理,处理的方法是:在d处将尾气点燃或在d处用气球收集尾气;
故答案为:(1)检验原气体样品中的二氧化碳是否除尽;(2)甲中药品由红变黑(或第一次通过乙石灰水不浑浊,第二次通过乙石灰水变浑浊);(3)有缺陷;在d处将尾气点燃(或在d处用气球收集尾气,合理给分).
(2)如果有一氧化碳,则一氧化碳能和氧化铁反应生成黑色的铁粉和二氧化碳,二氧化碳能使澄清的石灰水变浑浊.所以实验现象:甲中药品由红变黑或乙中石灰水第一次不变浑浊,第二次变浑浊,可以说明含有较多的一氧化碳;
(3)一氧化碳有毒,能够污染环境,要对尾气进行处理,处理的方法是:在d处将尾气点燃或在d处用气球收集尾气;
故答案为:(1)检验原气体样品中的二氧化碳是否除尽;(2)甲中药品由红变黑(或第一次通过乙石灰水不浑浊,第二次通过乙石灰水变浑浊);(3)有缺陷;在d处将尾气点燃(或在d处用气球收集尾气,合理给分).
点评:本题主要考查一氧化碳的还原性,以及实验设计能力,只有充分理解了一氧化碳的性质才能对相关方面的问题做出正确的判断.

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目