题目内容
(4分)写出碳与氧气反应的方程式: 、 。
C+O2=CO2; 2C+O2=2CO
解析试题分析:碳在氧气充足时燃烧生成二氧化碳,氧气不充足时燃烧生成一氧化碳。化学方程式为:C+O2 CO2(氧气充足); 2C+O2=
CO2(氧气充足); 2C+O2= 2CO(氧气不充足)
2CO(氧气不充足)
考点:碳的燃烧;充分燃烧与不充分燃烧。
点评:碳在氧气充足时充分燃烧生成二氧化碳,氧气不充足时不充分燃烧生成一氧化碳。

练习册系列答案
 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目
氮化铝(AlN)是新型的电子绝缘基片材料,用于大型和超大
型集成电路中.在高温下氮气、碳和三氧化二铝反应可以生成氮化铝微晶粉体和一氧化碳,用此方法制得的氮化铝中含有少量杂质碳和氧化铝.某校化学兴趣小组利用上述反应原理制取并测定所得样品中氮化铝的质量分数.
查阅资料:(1)Al2O3+2NaOH=2NaAlO2+H2O; (2)AlN+NaOH+H2O=NaAlO2+NH3↑.氨气易与酸反应.
设计实验:
实验一:制取氮化铝样品
实验二:测定所制氮化铝样品中氮化铝的质量分数
①按图2组装仪器,将9.1g氮化铝样品放入锥形瓶中,在分液漏斗中加入一定量的浓NaOH溶液
②称得盛有稀盐酸的烧杯和漏斗的总质量为200g
③打开止水夹C,从分液漏斗向锥形瓶中滴入浓NaOH溶液,直到不再产生气体为止
④打开止水夹B,从导管A处缓缓鼓入一定量的空气
⑤再次称量盛有稀盐酸的烧杯和漏斗的质量和为203.4g
⑥重复实验④⑤步骤后称得盛有稀盐酸的烧杯和漏斗的总质量仍为203.4g
实验讨论:(1)步骤①加入样品前还应检查 .
(2)装有碱石灰的干燥管作用是 ;装置中使用漏斗的目的是 .
(3)图2烧杯中稀盐酸不能换成浓盐酸的理由是 ;图2烧杯中稀盐酸不能换成浓硫酸的理由是 ;图2烧杯中稀盐酸能否换成稀硫酸 .
(4)步骤④的目的是 .
实验结论:所制氮化铝样品中氮化铝的质量分数为 %(写计算过程,4分).
事故处理:实验中,小明不小心将盛有约50mL的浓NaOH溶液打翻在桌面上.这时他应该采取的措施是: .
拓展探究:(1)实验后剩余的浓NaOH溶液 (能或不能)放回原试剂瓶,写出NaOH溶液露置在空气中发生的化学反应方程式 .
(2)本着节约药品的原则,同时又要确保实验顺利获得成功.则实验二中至少应准备40%浓NaOH溶液 g(写计算过程,4分).
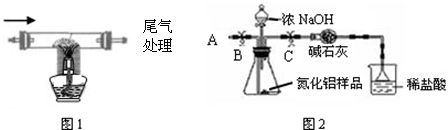
型集成电路中.在高温下氮气、碳和三氧化二铝反应可以生成氮化铝微晶粉体和一氧化碳,用此方法制得的氮化铝中含有少量杂质碳和氧化铝.某校化学兴趣小组利用上述反应原理制取并测定所得样品中氮化铝的质量分数.
查阅资料:(1)Al2O3+2NaOH=2NaAlO2+H2O; (2)AlN+NaOH+H2O=NaAlO2+NH3↑.氨气易与酸反应.
设计实验:
实验一:制取氮化铝样品
| 实验步骤 | 相关化学反应方程式 | ||||
| 1.除去空气中粉尘、二氧化碳、干燥后,再除去氧气. | 除去氧气的化学反应方程式为 2Cu+O2
| ||||
| 2.用上述制得的氮气通入装有碳和三氧化二铝硬质玻璃管中高温制取氮化铝样品(如图1). | 装置中发生化学反应的化学方程式为 N2+3C+Al2O3
|
①按图2组装仪器,将9.1g氮化铝样品放入锥形瓶中,在分液漏斗中加入一定量的浓NaOH溶液
②称得盛有稀盐酸的烧杯和漏斗的总质量为200g
③打开止水夹C,从分液漏斗向锥形瓶中滴入浓NaOH溶液,直到不再产生气体为止
④打开止水夹B,从导管A处缓缓鼓入一定量的空气
⑤再次称量盛有稀盐酸的烧杯和漏斗的质量和为203.4g
⑥重复实验④⑤步骤后称得盛有稀盐酸的烧杯和漏斗的总质量仍为203.4g
实验讨论:(1)步骤①加入样品前还应检查
(2)装有碱石灰的干燥管作用是
(3)图2烧杯中稀盐酸不能换成浓盐酸的理由是
(4)步骤④的目的是
实验结论:所制氮化铝样品中氮化铝的质量分数为
事故处理:实验中,小明不小心将盛有约50mL的浓NaOH溶液打翻在桌面上.这时他应该采取的措施是:
拓展探究:(1)实验后剩余的浓NaOH溶液
(2)本着节约药品的原则,同时又要确保实验顺利获得成功.则实验二中至少应准备40%浓NaOH溶液

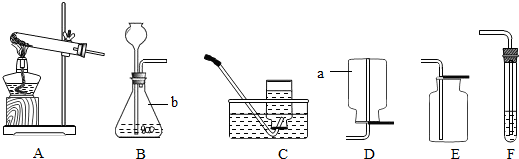
如图是实验室常用的实验仪器与装置,根据所学知识回答下列问题:
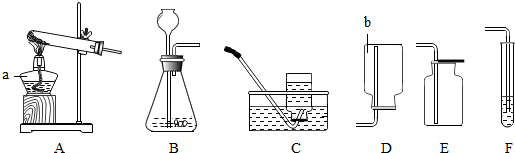
(1)请写出有编号的仪器名称:a b
(2)在实验室里,通常用下列方法制氧气:①双氧水和二氧化锰混合;②氯酸钾和二氧化锰混合加热;③加热高锰酸钾;其中最能体现“节能、环保、低碳”理念的制备方法是 (填序号),写出该反应的化学方程式: .
(3)当用A和C装置制取氧气时,发现水槽中的水变成紫红色,为避免此现象发生,应对该实验装置作出的一点改动是 .
(4)为检验CO2气体,可把气体通入F装置中,则F中的试剂是 ,F中反应的现象是 .
(5)阅读以下资料并回答:
制取氯气 (填“可以”或“不可以”,下同)采用B装置,收集氯气 采用E装置.

(1)请写出有编号的仪器名称:a
(2)在实验室里,通常用下列方法制氧气:①双氧水和二氧化锰混合;②氯酸钾和二氧化锰混合加热;③加热高锰酸钾;其中最能体现“节能、环保、低碳”理念的制备方法是
(3)当用A和C装置制取氧气时,发现水槽中的水变成紫红色,为避免此现象发生,应对该实验装置作出的一点改动是
(4)为检验CO2气体,可把气体通入F装置中,则F中的试剂是
(5)阅读以下资料并回答:
| 物质 | 制取气体的药品 | 反应条件 | 气体的物理性质 |
| 氯气 | 二氧化锰固体、 浓盐酸 |
需要加热 | 密度比空气大、 可溶于水 |
氮化铝(AlN)是新型的电子绝缘基片材料,用于大型和超大
型集成电路中.在高温下氮气、碳和三氧化二铝反应可以生成氮化铝微晶粉体和一氧化碳,用此方法制得的氮化铝中含有少量杂质碳和氧化铝.某校化学兴趣小组利用上述反应原理制取并测定所得样品中氮化铝的质量分数.
查阅资料:(1)Al2O3+2NaOH=2NaAlO2+H2O; (2)AlN+NaOH+H2O=NaAlO2+NH3↑.氨气易与酸反应.
设计实验:
实验一:制取氮化铝样品
| 实验步骤 | 相关化学反应方程式 |
| 1.除去空气中粉尘、二氧化碳、干燥后,再除去氧气. | 除去氧气的化学反应方程式为 2Cu+O2  2CuO 2CuO |
| 2.用上述制得的氮气通入装有碳和三氧化二铝硬质玻璃管中高温制取氮化铝样品(如图1). | 装置中发生化学反应的化学方程式为 N2+3C+Al2O3  2AlN+3CO 2AlN+3CO |
①按图2组装仪器,将9.1g氮化铝样品放入锥形瓶中,在分液漏斗中加入一定量的浓NaOH溶液
②称得盛有稀盐酸的烧杯和漏斗的总质量为200g
③打开止水夹C,从分液漏斗向锥形瓶中滴入浓NaOH溶液,直到不再产生气体为止
④打开止水夹B,从导管A处缓缓鼓入一定量的空气
⑤再次称量盛有稀盐酸的烧杯和漏斗的质量和为203.4g
⑥重复实验④⑤步骤后称得盛有稀盐酸的烧杯和漏斗的总质量仍为203.4g
实验讨论:(1)步骤①加入样品前还应检查______.
(2)装有碱石灰的干燥管作用是______;装置中使用漏斗的目的是______.
(3)图2烧杯中稀盐酸不能换成浓盐酸的理由是______;图2烧杯中稀盐酸不能换成浓硫酸的理由是______;图2烧杯中稀盐酸能否换成稀硫酸______.
(4)步骤④的目的是______.
实验结论:所制氮化铝样品中氮化铝的质量分数为______%(写计算过程,4分).
事故处理:实验中,小明不小心将盛有约50mL的浓NaOH溶液打翻在桌面上.这时他应该采取的措施是:______.
拓展探究:(1)实验后剩余的浓NaOH溶液______(能或不能)放回原试剂瓶,写出NaOH溶液露置在空气中发生的化学反应方程式______.
(2)本着节约药品的原则,同时又要确保实验顺利获得成功.则实验二中至少应准备40%浓NaOH溶液______g(写计算过程,4分).

氮化铝(AlN)是新型的电子绝缘基片材料,用于大型和超大
型集成电路中.在高温下氮气、碳和三氧化二铝反应可以生成氮化铝微晶粉体和一氧化碳,用此方法制得的氮化铝中含有少量杂质碳和氧化铝.某校化学兴趣小组利用上述反应原理制取并测定所得样品中氮化铝的质量分数.
查阅资料:(1)Al2O3+2NaOH=2NaAlO2+H2O; (2)AlN+NaOH+H2O=NaAlO2+NH3↑.氨气易与酸反应.
设计实验:
实验一:制取氮化铝样品
实验二:测定所制氮化铝样品中氮化铝的质量分数
①按图2组装仪器,将9.1g氮化铝样品放入锥形瓶中,在分液漏斗中加入一定量的浓NaOH溶液
②称得盛有稀盐酸的烧杯和漏斗的总质量为200g
③打开止水夹C,从分液漏斗向锥形瓶中滴入浓NaOH溶液,直到不再产生气体为止
④打开止水夹B,从导管A处缓缓鼓入一定量的空气
⑤再次称量盛有稀盐酸的烧杯和漏斗的质量和为203.4g
⑥重复实验④⑤步骤后称得盛有稀盐酸的烧杯和漏斗的总质量仍为203.4g
实验讨论:(1)步骤①加入样品前还应检查______.
(2)装有碱石灰的干燥管作用是______;装置中使用漏斗的目的是______.
(3)图2烧杯中稀盐酸不能换成浓盐酸的理由是______;图2烧杯中稀盐酸不能换成浓硫酸的理由是______;图2烧杯中稀盐酸能否换成稀硫酸______.
(4)步骤④的目的是______.
实验结论:所制氮化铝样品中氮化铝的质量分数为______%(写计算过程,4分).
事故处理:实验中,小明不小心将盛有约50mL的浓NaOH溶液打翻在桌面上.这时他应该采取的措施是:______.
拓展探究:(1)实验后剩余的浓NaOH溶液______(能或不能)放回原试剂瓶,写出NaOH溶液露置在空气中发生的化学反应方程式______.
(2)本着节约药品的原则,同时又要确保实验顺利获得成功.则实验二中至少应准备40%浓NaOH溶液______g(写计算过程,4分).
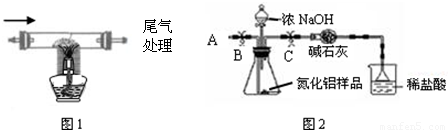
型集成电路中.在高温下氮气、碳和三氧化二铝反应可以生成氮化铝微晶粉体和一氧化碳,用此方法制得的氮化铝中含有少量杂质碳和氧化铝.某校化学兴趣小组利用上述反应原理制取并测定所得样品中氮化铝的质量分数.
查阅资料:(1)Al2O3+2NaOH=2NaAlO2+H2O; (2)AlN+NaOH+H2O=NaAlO2+NH3↑.氨气易与酸反应.
设计实验:
实验一:制取氮化铝样品
| 实验步骤 | 相关化学反应方程式 |
| 1.除去空气中粉尘、二氧化碳、干燥后,再除去氧气. | 除去氧气的化学反应方程式为 2Cu+O2 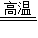 2CuO 2CuO |
| 2.用上述制得的氮气通入装有碳和三氧化二铝硬质玻璃管中高温制取氮化铝样品(如图1). | 装置中发生化学反应的化学方程式为 N2+3C+Al2O3 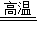 2AlN+3CO 2AlN+3CO |
①按图2组装仪器,将9.1g氮化铝样品放入锥形瓶中,在分液漏斗中加入一定量的浓NaOH溶液
②称得盛有稀盐酸的烧杯和漏斗的总质量为200g
③打开止水夹C,从分液漏斗向锥形瓶中滴入浓NaOH溶液,直到不再产生气体为止
④打开止水夹B,从导管A处缓缓鼓入一定量的空气
⑤再次称量盛有稀盐酸的烧杯和漏斗的质量和为203.4g
⑥重复实验④⑤步骤后称得盛有稀盐酸的烧杯和漏斗的总质量仍为203.4g
实验讨论:(1)步骤①加入样品前还应检查______.
(2)装有碱石灰的干燥管作用是______;装置中使用漏斗的目的是______.
(3)图2烧杯中稀盐酸不能换成浓盐酸的理由是______;图2烧杯中稀盐酸不能换成浓硫酸的理由是______;图2烧杯中稀盐酸能否换成稀硫酸______.
(4)步骤④的目的是______.
实验结论:所制氮化铝样品中氮化铝的质量分数为______%(写计算过程,4分).
事故处理:实验中,小明不小心将盛有约50mL的浓NaOH溶液打翻在桌面上.这时他应该采取的措施是:______.
拓展探究:(1)实验后剩余的浓NaOH溶液______(能或不能)放回原试剂瓶,写出NaOH溶液露置在空气中发生的化学反应方程式______.
(2)本着节约药品的原则,同时又要确保实验顺利获得成功.则实验二中至少应准备40%浓NaOH溶液______g(写计算过程,4分).