题目内容
下列物质分别与100g 36.5%的盐酸恰好完全反应,反应后所得溶液中溶质的质量分数最小的是( )
| A、Mg |
| B、MgO |
| C、Mg(OH)2 |
| D、MgCO3 |
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:溶质质量分数最小,若溶质相同时,所得的溶液质量最大时,溶质的质量分数最小.所以找出选项中所得溶液质量最大的就可以了.
解答:解:由Mg+2HCl=MgCl2+H2↑;
24 73
MgO+2HCl=MgCl2+H2O;
40 73
Mg(OH)2+2HCl=MgCl2+2H2O;
68 73
MgCO3+2HCl=MgCl2+H2O+CO2↑
84 73 44
可得出相同质量的盐酸与这四种物质完全反应后,生成的氯化镁的质量相同.
由盐酸和四种物质反应的关系可以看出,相同质量的盐酸消耗的碳酸镁质量最大,但碳酸镁与盐酸反应生成二氧化碳,氢氧化镁与盐酸反应不产生气体,所以相同质量的盐酸与四种物质反应时,所得溶液质量分数最小的是氢氧化镁.
故选C.
24 73
MgO+2HCl=MgCl2+H2O;
40 73
Mg(OH)2+2HCl=MgCl2+2H2O;
68 73
MgCO3+2HCl=MgCl2+H2O+CO2↑
84 73 44
可得出相同质量的盐酸与这四种物质完全反应后,生成的氯化镁的质量相同.
由盐酸和四种物质反应的关系可以看出,相同质量的盐酸消耗的碳酸镁质量最大,但碳酸镁与盐酸反应生成二氧化碳,氢氧化镁与盐酸反应不产生气体,所以相同质量的盐酸与四种物质反应时,所得溶液质量分数最小的是氢氧化镁.
故选C.
点评:氢氧化镁和碳酸镁与盐酸反应时,碳酸镁与盐酸反应生成二氧化碳,溶液增加的质量为碳酸镁的质量减二氧化碳的质量.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 如图是甲、乙两种物质的溶解度曲线.20℃时,向两支试管中加入等质量的甲、乙两种固体物质,分别加入10g水,使其充分溶解,观察到如图2所示的现象.下列说法正确的是( )
如图是甲、乙两种物质的溶解度曲线.20℃时,向两支试管中加入等质量的甲、乙两种固体物质,分别加入10g水,使其充分溶解,观察到如图2所示的现象.下列说法正确的是( )| A、20℃时,甲溶液是饱和溶液,乙溶液是不饱和溶液 |
| B、图1中a表示甲物质的溶解度曲线 |
| C、当乙中含有少量甲时,可用冷却热饱和溶液的方法提纯乙 |
| D、如图,保持20℃不变分别再加溶质,两溶液浓度均增大 |
下列各组物质中属于纯净物的一组是( )
| A、钱币、铜钟 |
| B、不锈钢、黄铜 |
| C、生铁、钢 |
| D、24 K金、铜导线 |
江苏省第18届运动会将于2014年9月19日在徐州市举行.为让徐州天更蓝、地更绿、水更清,下列市民建议不可行的是( )
| A、减少扬尘的排放,以防止雾霾天气 |
| B、推广使用太阳能,以减少化石燃料的使用 |
| C、回收有机垃圾,以开发综合利用 |
| D、提倡使用超薄塑料袋,以减少白色污染 |
把锌片放入CuSO4溶液中,锌片表面覆盖了一层红色物质,一会儿又有气泡冒出.同学们对此现象进行猜想和分析,其中没有科学依据的是( )
| A、甲认为红色物质是铜 |
| B、乙猜想CuSO4溶液呈酸性并验证 |
| C、丙认为锌的活动性比铜强 |
| D、丁推测气体是二氧化碳并检验 |
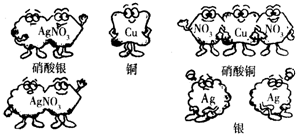 根据硝酸银溶液和铜反应的微观模拟图回答下列问题:
根据硝酸银溶液和铜反应的微观模拟图回答下列问题: