题目内容
【题目】“化学使天更蓝,水更清”.汽车尾气处理装置能使某些有毒气体转化为无毒气体:2NO+2CO N2+2CO2,该反应涉及的物质中:_____在空气中含量最高;_____是光合作用的原料;能与血红蛋白结合导致人体中毒的是_____。
N2+2CO2,该反应涉及的物质中:_____在空气中含量最高;_____是光合作用的原料;能与血红蛋白结合导致人体中毒的是_____。
【答案】氮气 二氧化碳 一氧化碳
【解析】
空气中各成分的体积分数分别是:氮气大约占78%、氧气大约占21%、稀有气体大约占0.94%、二氧化碳大约占0.03%、水蒸气和其它气体和杂质大约占0.03%;二氧化碳是光合作用的原料,能与血红蛋白结合的是一氧化碳,从而造成一氧化碳中毒。
空气中各成分的体积分数分别是:氮气大约占78%、氧气大约占21%,2NO+2CO N2+2CO2,该反应涉及的物质中:氮气在空气中含量最高;光合作用是利用二氧化碳和水生成葡萄糖和氧气,二氧化碳是光合作用的原料;能与血红蛋白结合导致人体中毒的是一氧化碳。
N2+2CO2,该反应涉及的物质中:氮气在空气中含量最高;光合作用是利用二氧化碳和水生成葡萄糖和氧气,二氧化碳是光合作用的原料;能与血红蛋白结合导致人体中毒的是一氧化碳。

 名校课堂系列答案
名校课堂系列答案【题目】(发现问题)小芳和她的化学兴趣小组对家用普通干电池中的黑色物质产生了兴趣,于是展开如下探究。
(提出问题)黑色物质的成分是什么?
(猜想与假设)查阅资料后,小芳发现黑色粉末里可能含有二氧化锰和炭粉。
(实验探究)小芳结合自己刚刚学过的知识,设计了利用过氧化氢溶液来验证黑色粉末的成分实验过程。
实验步骤 | 实验操作 | 实验现象 |
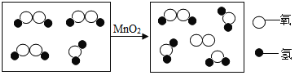
选择下图某装置为反应的发生装置,检查装置气密性,进行实验探究。 | 向反应容器中加入待探究的黑色粉末,将过氧化氢溶液加入反应容器中与黑色粉末混合,并将收集到的气体用带火星的木条验证。 | 带火星的木条复燃 |
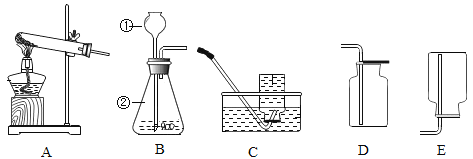
(1)写出仪器名称:①______________,②___________________;
(2)实验步骤中选用的发生装置是(填字母标号),该反应的符号表达式为_________,该反应的基本反应类型是___________;
(得出结论)黑色粉末中含有二氧化锰。
(反思评价)同组的小华觉得小芳的探究不全面,他觉得应该补充一个探究炭粉是否具有加快过氧化氢溶液反应速率的实验。
(3)结合学过的知识,自己设计实验证明黑色粉末中含有炭粉_____________________。
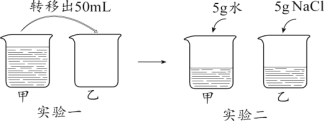
【题目】我市某校“绿色”环保小组的同学用精密酸度计测得实验室的甲、乙、丙、丁四种废液的pH如下表。现请你和他们一起实验并回答:
废液 酸碱度 | 甲 | 乙 | 丙 | 丁 |
pH | 6.5 | 11.3 | 7.0 | 2.0 |
(1)各取溶液少许,分别滴入1~2滴无色酚酞试液,能使酚酞试液变红的废液是_________________ 。
(2)实验老师告知:乙、丁分别是未用完的氢氧化钾溶液和稀盐酸。为了防止废液对环境的污染,小聪这一组将丁溶液逐滴滴入乙中,刚好完全反应,此时溶液的pH______7(填“<”、“>”、“=” ) 。该反应的化学方程式为:_____________________ 。
(3)小红这一组在做实验时忘了在乙溶液中滴加酚酞溶液,就滴加了丁溶液,这时立马又滴加了酚酞溶液,发现溶液是无色,此时老师让他们探究此时溶液中的溶质是什么?欢迎你也加入到这一组和他们一起探究,于是他们对溶液中的溶质进行了猜想:猜想1:溶质是氢氧化钾,猜想2:溶质是氯化钾,氯化氢,猜想3: __________ 。经过交流他们认为猜想1不正确你认为不正确的原因:_________。然后他们想了许多方法验证了猜想,请你完成下列实验
所用的方法 | 看到的现象 | 得出的结论 |
向反应的溶液中滴加紫色石蕊溶液 | 猜想2正确 | |
向反应的溶液中加入碳酸钠溶液 | 有较多的气泡产生 | 猜想2正确,写出反应的化学方程式____ |
【题目】金属、氧化物、酸、碱、盐之间能相互发生反应,某化学兴趣小组进行系列实验
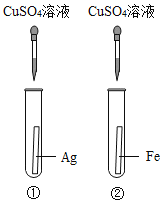
实验一:为探究铁、铜、银三种金属的活动性顺序,设计了A、B两个方案。
方案A | 方案B |
|
|
(1)能验证三种金属活动性顺序的方案是_____(填“A”或“B”)。
(2)方案B中,证明铁的活动性比铜强的现象是_____。
实验二:实验室用锌粒和稀硫酸反应制取氢气,若13克锌与足量的稀硫酸反应,计算产生氢气的物质的量。(根据化学方程式列式进行计算)_____
实验三:为研究碳酸钠、氢氧化钙、盐酸的化学性质,进行如下实验。
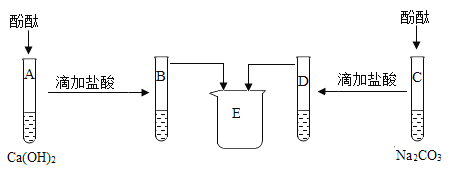
(1)A、C中酚酞均变_____色,证明Na2CO3和Ca(OH)2溶液呈碱性。
(2)B、D试管内的物质在烧杯E中混合产生白色沉淀,白色沉淀的化学式为_____,由此能否说明B中有反应物剩余?请你判断及说明理由_____,E中的溶质除酚酞外,一定含有的是_____(填化学式),可能含有的是_____(填化学式)。
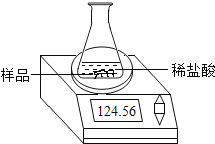
【题目】某化学兴趣小组为了粗略测定一批石灰石样品中CaCO3的质量分数,设计并进行如下实验。实验装置如图所示:称取研细的2.50g石灰石样品,分4次加入稀盐酸,充分反应至不再产生气体为止。测得反应前后的有关质量如表:
(1)反应生成二氧化碳的质量为_____。
(2)计算石灰石样品中CaCO3的质量分数_____。
(3)若在上述实验过程中石灰石样品和所加酸液均无抛洒,根据图中装置判断,该实验结果可能_____(填“偏大”、“偏小”或“准确”)。
反应前,整套装置+样品的质量/g | 共加入:稀盐 酸的质量/g | 反应后,整套装置+锥 形瓶中剩余物的质量/g |
104.60 | 20.00 | 123.72 |