��Ŀ����
����Ŀ����������������벻�������� 
��1�������ѣ�Ti���ĺϽ�����ܶ�С���۵�ߡ������Ժã�����ʴ��ǿ�����ܣ��ѺϽ��������кܺõġ������ԡ�����ҵ��ұ�������ѵĹ��������ѿ�ʯ����Ҫ�ɷ�Ϊ������������ѧʽΪFeTiO3������̿������Ϊԭ�ϣ��ڸ�����������ȡTiCl4 �� �䷴Ӧ�Ļ�ѧ����ʽΪ��2FeTiO3+6C+7Cl2![]() 2TiCl4+2X+6CO��Ȼ����þ��TiCl4 �� �ڸ��������·�Ӧ���ɽ����Ѻ��Ȼ�þ�������������Ϣ�ش��������⣺
2TiCl4+2X+6CO��Ȼ����þ��TiCl4 �� �ڸ��������·�Ӧ���ɽ����Ѻ��Ȼ�þ�������������Ϣ�ش��������⣺
��FeTiO3����Ԫ�صĻ��ϼ�Ϊ ��
����ȡTiCl4�ķ�Ӧ�У�X�Ļ�ѧʽΪ ��
��þ��TiCl4��Ӧ�Ļ�������Ϊ ��
�����й����ѺϽ���;��˵������ȷ���� ��
a��������˿ b�����ں��ա����칤ҵ c��������� d�����ڴ�������DZͧ������
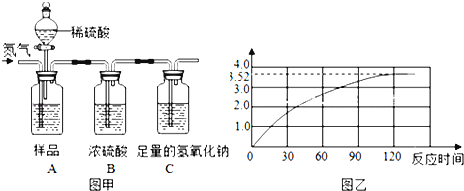
��2��ijС����ͼ1��ʾװ�ö����������������̽����һ��ʱ�����A�������������⣬B��������Ȼ�������Ա�A��B����˵�������������������һ����Ҫ������ ��
��3���ڽ����˳����У�����λ��Խ��ǰ��Խ����ʧȥ���ӣ�Ca��Mg��K���ֽ���ʧ����������ǿ������˳���� �� ��ͼ2������ԭ�ӵĽṹʾ��ͼ���ݴ��Ʋ����ʧ����������ǿ������Ԫ��ԭ�������������й��⣬���������йأ�
��4����¯��ʯ��ZnCO3������ͭ��Cu2O����ľ̿�ۻ�Ϻ���ȵ�Լ800�棬�õ�һ��п��ͭ�ĺϽ𩁩���ͭ������ƻƽ��ʵؼ�Ӳ������ʾ��ZnCO3���Ȼ�ֽ⣬���������������
��д����ͭ��ľ̿�۷�Ӧ�Ļ�ѧ����ʽ ��
���в��������û�ͭð��ƽ��Ƽ����ۣ����м�����ٻƽ�ķ�������ȷ���� ��
a������ b������� c���μ�ϡ���� d���μ���������Һ��
���𰸡�
��1��+4��FeCl3���û���Ӧ��a
��2��������Ũ��
��3��K��Ca��Mg��Ԫ��ԭ�Ӻ�����Ӳ���
��4��C+2Cu2O ![]() 4Cu+CO2����bd
4Cu+CO2����bd
����������1����FeTiO3����Ԫ�صĻ��ϼ�Ϊ+2����Ԫ�صĻ��ϼ�Ϊ��2������Ԫ�صĻ��ϼ�Ϊx�����У�+2��+x+����2����3=0��x=+4�����+4����2FeTiO3+6C+7Cl2![]() 2TiCl4+2X+6CO����Ӧǰ����2��Feԭ�ӣ�2��Tiԭ�ӣ�6��Oԭ�ӣ�6��Cԭ�ӣ�14��Clԭ�ӣ����ź���2��Tiԭ�ӣ�8��Clԭ�ӣ�6��Cԭ�Ӻ�6��Oԭ�ӣ���2X�к���2��Feԭ�ӣ�6��Clԭ�ӣ���X�Ļ�ѧʽΪFeCl3�����FeCl3����þ��TiCl4��Ӧ�����Ȼ�þ���ѣ������û���Ӧ������û���Ӧ�����ѺϽ���۵�ߣ����������Ʊ���˿�����a����2��������Ŀ�����������Ũ���йأ����������Ũ�ȣ���3��Ca��Mg��K���ֽ����Ļǿ��ΪK��Ca��Mg����ʧ����������ǿ������˳����K Ca Mg������ͼʾ���Կ�����ԭ��ʧ���ӵ���������Ԫ��ԭ�Ӻ�����Ӳ����йأ����K Ca Mg��Ԫ��ԭ�Ӻ�����Ӳ�������4����̼����������ͭ��Ӧ����ͭ�Ͷ�����̼��
2TiCl4+2X+6CO����Ӧǰ����2��Feԭ�ӣ�2��Tiԭ�ӣ�6��Oԭ�ӣ�6��Cԭ�ӣ�14��Clԭ�ӣ����ź���2��Tiԭ�ӣ�8��Clԭ�ӣ�6��Cԭ�Ӻ�6��Oԭ�ӣ���2X�к���2��Feԭ�ӣ�6��Clԭ�ӣ���X�Ļ�ѧʽΪFeCl3�����FeCl3����þ��TiCl4��Ӧ�����Ȼ�þ���ѣ������û���Ӧ������û���Ӧ�����ѺϽ���۵�ߣ����������Ʊ���˿�����a����2��������Ŀ�����������Ũ���йأ����������Ũ�ȣ���3��Ca��Mg��K���ֽ����Ļǿ��ΪK��Ca��Mg����ʧ����������ǿ������˳����K Ca Mg������ͼʾ���Կ�����ԭ��ʧ���ӵ���������Ԫ��ԭ�Ӻ�����Ӳ����йأ����K Ca Mg��Ԫ��ԭ�Ӻ�����Ӳ�������4����̼����������ͭ��Ӧ����ͭ�Ͷ�����̼��
���C+2Cu2O ![]() 4Cu+CO2������a������ʱ�ٻƽ��е�ͭ����������Ӧ���ɺ�ɫ������ͭ�����Լ���b���������ɫһ����������c���μ�ϡ����ٻƽ��е�п�������ᷴӦ�������������Լ���d���μ���������Һ���ᷴӦ�����ܼ��𣮹��bd��
4Cu+CO2������a������ʱ�ٻƽ��е�ͭ����������Ӧ���ɺ�ɫ������ͭ�����Լ���b���������ɫһ����������c���μ�ϡ����ٻƽ��е�п�������ᷴӦ�������������Լ���d���μ���������Һ���ᷴӦ�����ܼ��𣮹��bd��
�����㾫�������ս������ϵ�ѡ�����ݺ���д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ�ǽ����ĸ�������Ҫ֪����ɫ������ͨ��ָ�����̡��������ǵĺϽ��ؽ�������ͭ��п��Ǧ�ȣ���ɫ��������������ơ�þ�����ȣ���ɫ������ͨ����ָ����ɫ�������������������ע�⣺a����ƽ b������ c�����ţ�