题目内容
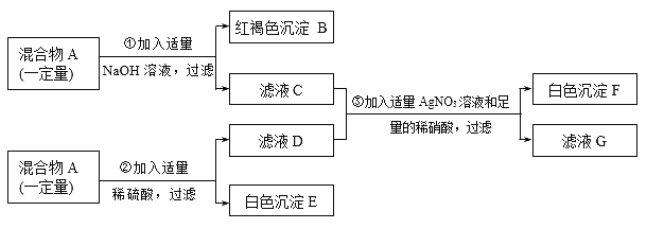
【题目】海水中含有丰富的资源,下图是从海水中提取镁的简单流程。

(1)操作①的名称为____。
(2)沉淀B与试剂C发生中和反应,该反应的化学方程式为![]() ____________。
____________。
(3)由无水![]()
![]() 电解制取Mg的化学反应方程式为____________。其基本反应类型_______
电解制取Mg的化学反应方程式为____________。其基本反应类型_______
【答案】 过滤 Mg(OH)2+2HCl=MgCl2+2H2O MgCl2![]() Mg +Cl2↑ 分解反应
Mg +Cl2↑ 分解反应
【解析】先加氢氧化钠使镁离子沉淀,要使镁离子全部转化加的氢氧化钠必须过量。镁离子富聚后再加盐酸,溶解沉淀得到MgCl2溶液,干燥后再电解得到单质镁。
解:(1)操作①后得到固体和液体,故(1)操作①的名称为过滤;
(2)沉淀B是氢氧化镁,试剂C是稀盐酸,故该反应的化学方程式为Mg(OH)2+2HCl=MgCl2+2H2O;
(3) 由无水MgCl2电解制取Mg的化学反应方程式为MgCl2通电 Mg +Cl2↑;基本反应类型是分解反应。

练习册系列答案
相关题目