题目内容
(2012?镇江)现有一包白色固体粉末,可能含有CuSO4、Na2SO4、CaCO3、BaCl2、KCl中的一种或几种,现做如下实验:
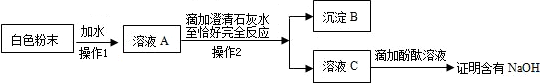
(1)取少量白色固体加入足量的水溶解,过滤得固体和无色溶液.
(2)向所得固体中加入足量的稀盐酸,固体部分溶解,并有气体产生.
根据上述实验现象判断:
①白色固体中一定不含
②写出(2)中固体部分溶解的反应化学方程式
(1)取少量白色固体加入足量的水溶解,过滤得固体和无色溶液.
(2)向所得固体中加入足量的稀盐酸,固体部分溶解,并有气体产生.
根据上述实验现象判断:
①白色固体中一定不含
CuSO4
CuSO4
,一定含有Na2SO4、CaCO3、BaCl2
Na2SO4、CaCO3、BaCl2
,可能含有KCl
KCl
.②写出(2)中固体部分溶解的反应化学方程式
CaCO3+2HCl═CaCl2+H2O+CO2↑
CaCO3+2HCl═CaCl2+H2O+CO2↑
.分析:该类题中往往会有明显的现象特征,解题时就以此为突破口.
(1)中题眼有“上层溶液为无色”,“白色沉淀”.
(2)中“白色沉淀部分溶于稀盐酸”中的“部分溶于”,“无色气体”,抓住这些题眼可快速解答.
(1)中题眼有“上层溶液为无色”,“白色沉淀”.
(2)中“白色沉淀部分溶于稀盐酸”中的“部分溶于”,“无色气体”,抓住这些题眼可快速解答.
解答:解:固体粉末加到水中,得到白色沉淀,且上层清液为无色,说明粉末中一定没有硫酸铜,白色沉淀可能是碳酸钙或硫酸钠与氯化钡反应产生的硫酸钡;白色沉淀部分溶于稀盐酸,说明沉淀为碳酸钙和硫酸钡,因为碳酸钙溶于盐酸并与盐酸反应生成氯化钙水和二氧化碳,而硫酸钡不溶于盐酸,也不能与盐酸反应,因此一定含有碳酸钙、硫酸钠和氯化钡,氯钾可能含有.
故答案为:①CuSO4;Na2SO4、CaCO3、BaCl2;KCl;
②CaCO3+2HCl═CaCl2+H2O+CO2↑;
故答案为:①CuSO4;Na2SO4、CaCO3、BaCl2;KCl;
②CaCO3+2HCl═CaCl2+H2O+CO2↑;
点评:本题属于文字叙述型推断题,给出物质范围和实验现象,要求考生推出混合物中一定存在、一定不存在和可能存在的是什么物质.解答时以文字信息为序,寻找并抓住“题眼”,逐步分析“筛选”.这就要求考生熟悉这类题目的常见“题眼”,也就是解题的“突破口”.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
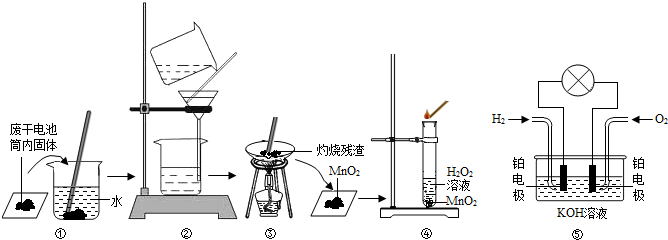
 (1)B俗称
(1)B俗称