题目内容
【题目】化学兴趣小组对某品牌牙膏中碳酸钙含量进行以下探究。该牙膏摩擦剂主要由碳酸钙、氢氧化铝组成,其他成分遇到盐酸时无气体生成。现利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定B中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。请回答下列问题。(已知:碱石灰固体的主要成分是生石灰和烧碱)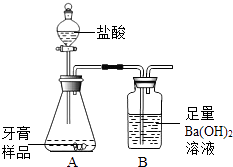
(1)装置A中牙膏样品放置在(填仪器名称)中,盐酸放置在装置(填仪器名称)中,A中至少发生(填数字)个反应,写出其中一个反应的化学方程式
(2)若测定值比实际值小,可能的原因有(填字母)a.装置A中水蒸气、HCl等进入装置B中
b.装置A中CO2未完全进入装置B
c.CO2气流速度太快导致Ba(OH)2未完全吸收
d.盐酸未滴加过量
(3)为减少误差,现采取以下一些措施:①在A、B之间增加一个装有(填化学式)溶液的洗气瓶,它的作用是;
②若将装置B中的长导管下方增加一个多孔球泡,作用是;
③若将装置A的前面再增加一个鼓入氮气的装置,目的是;
④若在装置B的后面再增加一个装有碱石灰固体的干燥管,目的是。
(4)准确称取三份各16.00g的样品,进行测定,测得BaCO3质量分别为3.96g、3.92g、3.94g。请计算样品中碳酸钙的质量分数。(写出计算过程)
(5)某同学利用上述方法测定牙膏中钙元素的质量分数。小李同学认为即使排除实验仪器和操作的影响,上述测定的结果仍有可能偏小,理由是:。
【答案】
(1)锥形瓶;分液漏斗;2;CaCO3+2HCl═CaCl2+H2O+CO2↑
(2)bcd
(3)硝酸银;吸收HCl,防止进入B装置;增大接触面积,提高吸收效率;使残留在装置内的CO2完全进入装置B,被充分吸收;吸收空气中的二氧化碳防止进入装置B(只答吸水吸二氧化碳不得分,至少答到吸收空气中的二氧化碳)
(4)解:设碳酸钙的质量为x,
三份BaCO3的平均质量为3.94g
CaCO3~~~~ | CO2 ~~~~ | BaCO3 |
100 | 44 | 197 |
x | 3.94g |
![]()
x=2g
CaCO3的质量分数= ![]() ×100%=12.5%
×100%=12.5%
(5)牙膏中可能含有其他含钙物质
【解析】(1)如图,固体与液体反应时,固体放在锥形瓶中,液体从长颈漏斗加入;该牙膏摩擦剂主要由碳酸钙、氢氧化铝组成,两物质都能与盐酸发生反应,所以A中至少发生两个反应,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,氢氧化铝与盐酸反应生成氯化铝和水;(2)a.装置A中水蒸气、HCl等进入装置B中,会因测得的二氧化碳质量偏大而使得测定值比实际值偏大;b.装置A中CO2未完全进入装置B,会使得测定值比实际值小;c.CO2气流速度太快导致Ba(OH)2未完全吸收测定值比实际值小;d.盐酸未滴加过量使碳酸钙没有完全反应,测定值比实际值小;(3)因盐酸有挥发性,挥发出的氯化氢影响测得结果,所以A、B之间增加一个吸收氯化氢的装置,如硝酸银溶液;若将装置B中的长导管下方增加一个多孔球泡,可以增大药品的接触面积,提高吸收效率;因有气体生成的反应装置内会残留气体,所以可在将装置A的前面再增加一个鼓入氮气的装置,使残留在装置内的CO2完全进入装置B,被充分吸收;若在装置B的后面再增加一个装有碱石灰固体的干燥管,可吸收空气中的二氧化碳防止进入装置B影响测定结果。(5)因牙膏中可能含有其他含钙物质,所以利用上述方法测定牙膏中钙元素的质量分数即使排除实验仪器和操作的影响,测定的结果仍有可能偏小。
【考点精析】本题主要考查了书写化学方程式、文字表达式、电离方程式和根据化学反应方程式的计算的相关知识点,需要掌握注意:a、配平 b、条件 c、箭号;各物质间质量比=系数×相对分子质量之比才能正确解答此题.