题目内容
【题目】为了探究石灰石与稀盐酸反应制备二氧化碳后的废液中的溶质成分,将废液过滤,取滤液224.4克于烧杯中,在不断振荡的条件下,向其中逐滴加质量分数为10.6%的碳酸钠溶液直至过量,有关的变化如图所示。经测定A中只含有一种溶质。根据题中有关信息和图像分析回答下列问题。
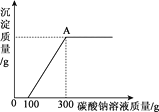
(1)原废液中的溶质成分有________(用化学式回答)
(2)该碳酸钠溶液中钠元素的质量分数为_________(结果保留到0.1%)
(3)A点处溶液中溶质的质量分数是多少?(列出必要的解题步骤,结果保留到0.1%)
【答案】(1)CaCl2,HCl;(2)4.6%;(3)6.1%
【解析】由题中信息知,(1)原废液中的溶质成分有CaCl2,HCl;
(2)碳酸钠相对分子质量是106,Na2CO3→2 Na.106→46,该碳酸钠溶液中钠元素的质量分数为4.6%;(3)A点处溶液中溶质的质量分数是∶
Na2CO3+2HCl=2NaCl+CO2 ↑+H2O
106 117 44
100g×10.6% x z
![]() =
=![]() ,x=11.7g.
,x=11.7g. ![]() =
=![]() ,z=4.4g.
,z=4.4g.
Na2CO3+CaCl2=Ca2CO3 ↓+2NaCl
106 100 117
200g× 10.6% z y
![]() =
= ![]() ,y=23.4g .
,y=23.4g . ![]() =
= ![]() ,z=20g.
,z=20g.
A点处溶液中溶质的质量分数是∶![]() ×100%=6.1%.
×100%=6.1%.
答∶ (1)原废液中的溶质成分有CaCl2,HCl;
(2)该碳酸钠溶液中钠元素的质量分数为4.6%;
(3)A点处溶液中溶质的质量分数是6.1%.
点睛∶本题主要考查质量守恒定律的应用以及根据化学方程式进行计算。

练习册系列答案
相关题目