题目内容
【题目】(5 分)海洋是一座巨大的宝库,海水中蕴含着 80 多种元素。氯碱工业就是以海水为原材料来大量制取烧碱和氯气。烧碱和氯气是重要的化工生产原料,可以进一步加工成多种化工产品,广泛用于工业生产。(1)氯碱工业中发生反应的化学方程式为:2NaCl + 2H2O=2NaOH + Cl2↑+A, 则 A的化学式为 。
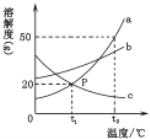
(2)下图是甲、乙两种固体物质的溶解度曲线。
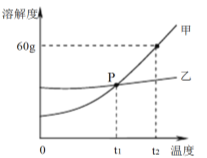
①P 点的意义是 。
②甲物质中含有少量乙物质,可用 的方法提纯甲(选填“降温结晶”、“蒸发结晶”之一),叙述提纯的原理____________________________________。
【答案】(1)H2 (2)①t1℃时,甲乙两物质的溶解度相等。②降温结晶 甲物质的溶解度随温度升高明显增大,而乙物质溶解度受温度的变化影响小 。降温时,甲物质溶解度明显变小,其饱和溶液中会有大量结晶析出,而乙不会。
【解析】
试题分析:(1)氯碱工业中发生反应的化学方程式为:2NaCl + 2H2O=2NaOH + Cl2↑+A,根据质量守恒定律,反应前后原子的种类和数量不变,则 A的化学式为H2 (2)由溶解度曲线图可知① P 点的意义是在 t1℃,甲乙两物质溶解度相等;② 甲物质中含有少量乙物质,提纯甲物质,根据溶解度曲线甲物质的溶解度随温度的升高而增大较大,故可用降温结晶的方法;

练习册系列答案
相关题目