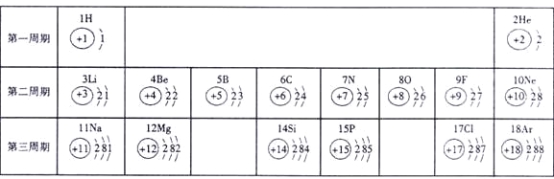
��Ŀ����
����Ŀ��Ϊ�˷�ֹ��Ⱦ���û�ͭ��(��Ҫ�ɷ��� CuFeS2��������Zn�Ļ�����)��ͭʱ���������ķ�������Һת���ɹ�ҵԭ�ϣ�����������£�(�ٶ�ÿһ������ȫ��Ӧ)
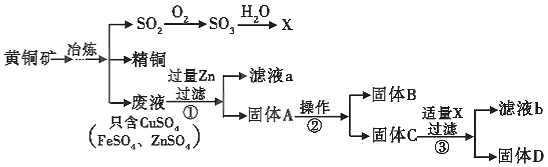
(1)����������õ��IJ�ƷX��_____��
(2)д��������з�Ӧ�Ļ�ѧ����ʽ_____��
(3)����ڵIJ�����_____��
(4)��Һa����Һb�����ʵijɷ�_____(������ͬ����������ͬ��)��
(5)���������������ʵ���ʧ���Բ��ƣ�Ҫ����2.8g B��3.2gD�������Zn������Ӧ���ٴ���_____g��
���𰸡�H2SO4Zn+CuSO4=Cu+ZnSO4��Zn+FeSO4=Fe+ZnSO4�ô���������ͬ6.5
��������
��1������������ˮ��Ӧ���������ᣬ��X��H2SO4 ��
��2��п������ͭ���ã��ʽ�п��������ͭ����������������п�Ļ����Һ�к�п����������������ͭ���Է�Ӧ����Ӧ����ʽΪZn+CuSO4=Cu+ZnSO4��Zn+FeSO4=Fe+ZnSO4 ��
��3������2�ǽ����ֲ�ͬ�Ľ�������Ĺ����������Ա�������������п��ͭ���ܱ����������������ô��������ʹ���B����������C��п��ͭ�Ļ������
��4����Һa�ǹ�����п������ͭ�����������IJ����������п������A�ǹ�����п�����ɵ�����ͭ�Ļ���������������������ʹ���B����������C��п��ͭ�Ļ�����п��ͭ�Ļ�����м���ϡ���ᣬп������ϡ���ᷴӦ����������п��������ͭ����ϡ���ᷴӦ���ʹ���D��ͭ��Һb������п������Һa����Һb��������ͬ��
��5��������2.8g������Ҫп������Ϊx������3.2gͭ��Ҫп������Ϊy
Zn+CuSO4=Cu+ZnSO4��Zn+FeSO4=Fe+ZnSO4
65 64 65 56
y 3.2g x 2.8g
![]() =
=![]() ��
��![]() =
=![]() ��x=3.25g��y=3.25g��3.25g+3.25g=6.5g
��x=3.25g��y=3.25g��3.25g+3.25g=6.5g

 ��Ȥ����¹�֪��ϵ�д�
��Ȥ����¹�֪��ϵ�д� Ӣ��СӢ������Ĭдϵ�д�
Ӣ��СӢ������Ĭдϵ�д�����Ŀ���������(KClO4)����������ƽ��������ܽ�����±�������˵������ȷ����( )
�¶�/�� | 20 | 40 | 60 | 80 |
�ܽ��/g | 1.68 | 3.73 | 7.3 | 13.4 |
A. ������ص��ܽ�����¶Ƚ��Ͷ���С
B. 80���ĸ�����ر�����Һ��ȴ��40��һ���о�������
C. 60��ʱ��������ر�����Һ�����ʵ���������С��7.3%
D. 20��ʱ����2g��������м���98gˮ��������Һ��������������Ϊ2%