题目内容
【题目】请结合图示实验装置,回答下列问题.

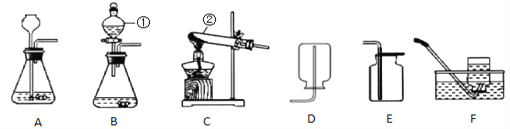
(1)写出有标号的仪器名称:②________________
(2)实验室用高锰酸钾制氧气选用的发生装置是_____(填序号),反应的化学方程式为____________________________________
(3)实验室可用B或C装置制CO2,反应的化学方程式为_____________________,C相对于B装置的优点有_________________________
(4)实验室可用F装置组合测量生成二氧化碳的体积,导管b的作用是________________;植物油的作用是___________________。
(5)若B装置中固体为锌粒,②中加入浓盐酸制H2.欲获得纯净干燥的氢气需经过两次D装置,第一个D装置中应盛放的试剂是_________________溶液,第二个D装置中应盛放的试剂是_______________ (填名称),再用E装置收集H2,气体应从________端通入(选填“a”或“b”)
【答案】 分液漏斗 A 略 略 控制反应的发生与停止(随开随停) 保持内外压力平衡 防止二氧化碳溶于水 NaOH(氢氧化钠) 浓硫酸 a
【解析】(1)由图可知,②是分液漏斗;(2)根据反应物的状态和反应条件选择发生装置,用加热高锰酸钾的方法制取氧气属固固加热型,发生装置选A;加热高锰酸钾分解制取氧气的同时,还生成了锰酸钾和二氧化锰,故反应的化学方程式是2KMnO4 △K2MnO4 +MnO2 + O2↑;(3)实验室用石灰石或大理石和稀盐酸反应制取二氧化碳,同时还生成了氯化钙和水,反应的化学方程式表示为CaCO3 + 2HCl == CaCl2 + H2O + CO2↑;B装置的优点是分液漏斗可以控制加入液体药品的量和速率来控制其反应速率;C装置中可将石灰石放在多孔隔板上,稀盐酸从长颈漏斗中加入,当不需要反应时,用止水夹夹住橡皮管,稀盐酸进入到长颈漏斗中,石灰石和稀盐酸分离,反应停止,故C装置的优点是能控制反应的发生和停止;(4)导管b能保持内外压力平衡,使稀盐酸更易加入;二氧化碳易溶于水,故植物油的作用是防止二氧化碳溶于水;(5)浓盐酸具有挥发性,要收集到纯净的氢气,那么要把氯化氢气体除去,可用氢氧化钠溶液除去氯化氢气体;由于氢氧化钠溶液中含有水,那么通过氢氧化钠溶液后的氢气含有水蒸气,将氢气通过浓硫酸即可除去水蒸气;氢气的密度比空气小,会先聚集在集气瓶的上部,故氢气应从a端通入。

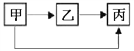
【题目】下表所列各组物质中,物质之间按箭头方向通过一步反应不能全部实现如图所示转化的是
物质 选项 | 甲 | 乙 |
|
A. | Fe2O3 | CO2 | H2O |
B. | C | CO | CO2 |
C. | CaCO3 | CaO | Ca(OH) 2 |
D. | H2SO4 | H2O | H2 |
A. A B. B C. C D. D