题目内容
【题目】以下是初中化学的一些基本实验,根据图示回答问题。
A 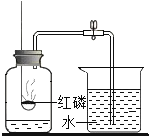 测定空气中O2含量
测定空气中O2含量
B 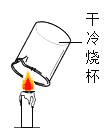 探究蜡烛的元素组成
探究蜡烛的元素组成
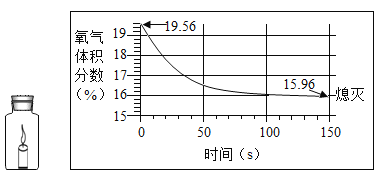
C 铁丝在空气中中的变化
铁丝在空气中中的变化
(1)A中集气瓶内水的作用是_____________________________________________。
(2)B中得出的实验结论是_____________________________。
(3)一段时间后,C中的实验现象为_______________,产生该现象的原因是______________________。
【答案】吸收白烟,冷却降温 蜡烛中含有氢元素 铁丝表面变红,U型管液面a上升b下降 由于铁与氧气和水反应生成铁锈,造成内部气体减少,压强降低,导致外界大气将b侧液体压向a侧,a侧液位高于了b侧;
【解析】
(1)磷与氧气反应生成五氧化二磷,形成白烟,属于有毒物质,不能直接排放,所以加入水进行吸收,避免污染环境,同时,反应属于放热反应,水可以吸收热量,利用瓶内降温;
故答案为:吸收白烟,冷却降温。
(2)烧杯内会有水滴出现,说明反应中有水生成,生成物含有氢和氧两种元素,空气中蜡烛燃烧是与氧气反应,所以反应物中有了氧元素,根据质量守恒定律,氢元素来自于蜡烛,所以此实验可以证明蜡烛中含有氢元素;
故答案为:蜡烛中含有氢元素。
(3)铁与氧气和水接触,满足铁生锈的条件,所以铁丝生锈,表面变红,由于内部气体的减少,压强降低,所以外界大气压将b侧液体压向a侧,造成a侧液位高于b侧,所以可以看到铁丝生锈,表面变红,a侧液位高于b侧,由于铁与氧气和水反应生成铁锈,造成内部气体减少,压强降低,导致外界大气将b侧液体压向a侧,a侧液位高于了b侧;
故答案为:铁丝表面变红,U型管液面a上升b下降;由于铁与氧气和水反应生成铁锈,造成内部气体减少,压强降低,导致外界大气将b侧液体压向a侧,a侧液位高于了b侧。

【题目】下列图像能正确反映实验过程中相应量变化的是
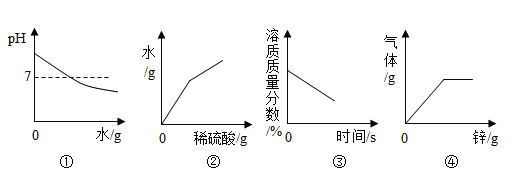
A.图①:向氢氧化钠溶液中加水
B.图②:向氢氧化钡溶液中加足量稀硫酸
C.图③:将接近饱和的硝酸钾溶液缓慢降温
D.图④:向一定量的稀硫酸中加入过量的锌
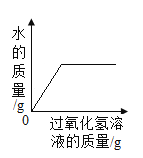
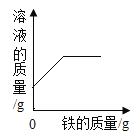
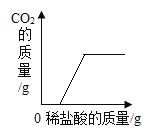
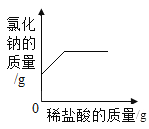
【题目】下列4个坐标图分别表示4个实验过程中某些物质质量的变化,其中正确的是()
A | B | C | D |
向一定量二氧化锰中滴加过氧化氢溶液 | 向一定量硫酸铜溶液中不断加入铁粉 | 向一定量大理石中滴加稀盐酸 | 向一定量氯化钠和碳酸氢钠混合物中滴加稀盐酸 |
|
|
|
|
A.AB.BC.CD.D
【题目】化学小组同学在课外读物中看到:“加热时,过氧化钠(Na2O2)能与木炭发生化学反应”。他们决定探究Na2O2与木炭反应的产物。
(猜想与假设)木炭与Na2O2反应可能生成4种物质:CO、CO2、Na2O和Na2CO3。
(查阅资料)
① 碱性的碳酸钠溶液与中性的CaCl2溶液能发生复分解反应。
② 氧化钠(Na2O)是白色固体,与H2O反应生成NaOH。
③ 氯化钯(PdCl2)溶液能检验CO的存在,向溶液中通入CO,产生黑色沉淀。
(进行实验)同学们在老师的指导下设计了如下图所示装置(部分夹持仪器已略去)。
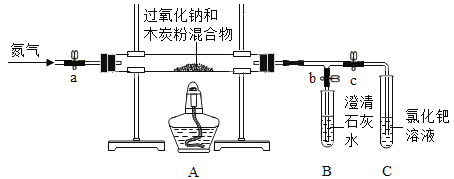
序号 | 实验操作 | 主要实验现象 | 实验结论 |
① | 检查装置气密性。向玻璃管中加入过氧化钠和过量木炭粉的混合物。打开弹簧夹a、b,关闭c,从装置左端通一段时间N2。 | A中无明显变化,B中有大量气泡冒出。 | 气密性良好。 |
② | 关闭a,点燃酒精灯。 | 试管中发生剧烈反应,产生火花,________________。 | 产物中没有CO2。 |
③ | 打开c,关闭b。 | C中PdCl2溶液没有明显变化。 | ___________________。 |
④ | 打开a,继续通N2,停止加热,待冷却后停止通N2。取出少量反应后固体于试管中,加入足量稀盐酸,迅速用带导管的橡胶塞塞紧试管口,导管另一端通入石灰水中。 | _____________________。 | 产物中有Na2CO3。 |
(解释与结论)
(1)检验第4种物质存在的实验方案:取出少量反应后固体于试管中,_______________,则第4种物质存在。
(2)Na2O2与木炭反应的化学方程式为_________________________________。
(反思与评价)实验操作④中若不通入N2,可能造成的结果是________________________。