��Ŀ����
����Ŀ�����ƻ�ѧ��Ӧ���������Դٽ������ƻ�ѧ��Ӧ������ʹ��ѧ��ӦΪ�����츣��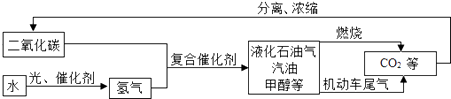
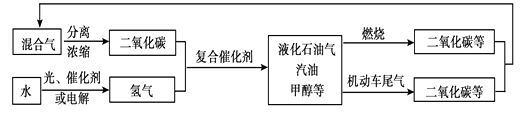
��1����ͼ�ǿ�ѧ�������о��Ķ�����̼ѭ�����ü�����
�ٶ�����̼�������ڴ��������������£������ɼ״���CH4O���⣬������һ�ֳ�����ΪҺ̬�Ļ����д����Ӧ�Ļ�ѧ����ʽ �� �״���̼Ԫ�صĻ��ϼ�Ϊ ��
�ڴ�ͼ�з����ó������н����У���ȷ����������ţ�
A���ü������ϵ�̼���õ�����
B��ˮ���������Ĺ��������õĴ���һ���Ƕ�������
C���ü��������ڻ���ȫ�����ٵ���ԴΣ��
D��Һ��ʯ���������͡��״�����̼���⡢������Ԫ�����
��2���������п�ѭ��ʹ�õ�������
��3������[CO(NH2)2]�������ʳ����������Ҫ�����ã����ǿ�����������ʹCO2������M������Ӧ��CO2 + 2M �T CO(NH2)2+ H2O������M�Ļ�ѧʽΪ��
���𰸡�
��1��CO2+3H2=CH4O+H2O,-2��,A��C
��2��CO2��H2O
��3��NH3
���������⣺�ٶ�����̼���������ɼ״���CH3OH����ˮ����ѧ����ʽ��CO2 + 3H2 = CH4O + H2O����״���̼Ԫ�صĻ��ϼ�Ϊx����x+1��3��2+1=0��x=��2����A��������̼ѭ�����ã����ϵ�̼���õ����A�������⣻B��ˮ���������Ĺ��������õĴ�����һ���Ƕ������̣�B���������⣻C��������̼ѭ�����ã��ü��������ڻ���ȫ�����ٵ���ԴΣ����C�������⣻D��Һ��ʯ���������͡��״��������й�����̼���⡢������Ԫ�أ�D���������⣻��2���������п�ѭ��ʹ�õ�������CO2��H2O����3�����������غ㶨�ɣ���ѧ��Ӧǰ��ԭ�ӵ��������Ŀ���䣬��ӦǰC��Oԭ�Ӹ�����1��2����Ӧ��C��O��N��Hԭ�Ӹ�����1��2��2��6��������M�Ļ�ѧʽΪNH3��
���Դ��ǣ���1��CO2+3H2=CH4O+H2O��-2�ۣ�A��C����2��CO2��H2O����3��NH3��
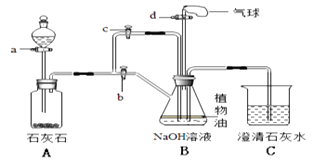
�����㾫�������������غ㶨�ɼ���Ӧ�ú���д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ����Ŀ�����жϼ��ɵõ��𰸣���Ҫ��֪�������غ㶨��ֻ�����ڻ�ѧ�仯���������������仯���ڲ��μӷ�Ӧ����������������������������������ܼ��롰�ܺ͡��У���Ҫ���ǿ����е������Ƿ�μӷ�Ӧ�����ʣ������壩������©��ע�⣺a����ƽ b������ c�����ţ�

 �Ƹ�С״Ԫ����������ϰ��ϵ�д�
�Ƹ�С״Ԫ����������ϰ��ϵ�д� �ɹ�ѵ���ƻ�ϵ�д�
�ɹ�ѵ���ƻ�ϵ�д� ����ѵ����ֱͨ�п�����ϵ�д�
����ѵ����ֱͨ�п�����ϵ�д� һ���㶨ϵ�д�
һ���㶨ϵ�д� ��У��ҵ��ϵ�д�
��У��ҵ��ϵ�д�