题目内容
【题目】兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验。请你与他们一起完成以下探究活动:
【对固体猜想】
猜想Ⅰ:全部是NaOH;猜想Ⅱ:全部是Na2CO3;猜想Ⅲ:是NaOH和Na2CO3混合物。
【实验和推断】
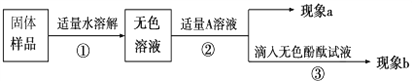
(1)若现象a为有气泡产生,则加入的A溶液是_____________,说明氢氧化钠已经变质。
(2)若A是Ca(OH)2溶液,现象a有白色沉淀,现象b为无色酚酞试液变红色,则白色沉淀为_________(填化学式),该实验________(填“能千或“不能”)说明样品中有NaOH。
(3)若A是CaCl2溶液,当实验现象a为_______________________________________,现象b为______________________________________________________,则猜想Ⅱ成立。
【反思】久置的氢氧化钠变质的原因是(用化学方程式表示)_________________________。
【答案】 盐酸 CaCO3 不能 有白色沉淀产生 无色酚酞不变红色 CO2+2NaOH=Na2CO3+H2O
【解析】根据所学知识和题中信息知,【对固体猜想】猜想Ⅰ:全部是NaOH;猜想Ⅱ:全部是Na2CO3;猜想Ⅲ:是NaOH和Na2CO3混合物。【实验和推断】(1)若现象a为有气泡产生,则加入的A溶液是盐酸,说明氢氧化钠已经变质,盐酸与碳酸钠反应。(2)若A是Ca(OH)2溶液,现象a有白色沉淀,现象b为无色酚酞试液变红色,则白色沉淀为CaCO3 ,该实验不能明样品中有NaOH。(3)若A是CaCl2溶液,当实验现象a为有白色沉淀产生,现象b为无色酚酞不变红色,则猜想Ⅱ成立。【反思】久置的氢氧化钠变质的原因是CO2+2NaOH=Na2CO3+H2O。
点睛∶本题主要考查探究实验室中久置的氢氧化钠固体的成分。

【题目】某兴趣小组同学对NaOH、Na2CO3、NaHCO3、NaCl等常见的钠的化合物进行了研究。
【知识回顾】下列相关说法正确的是____。
A.氢氧化钠俗名叫烧碱,可用于改良酸性土壤 B.碳酸钠俗称纯碱,属于碱
C.碳酸氢钠俗称苏打,可用于治疗胃酸过多 D.氯化钠在自然界中主要存在于海水中
【提出问题】NaOH露置于空气中易变质,那么实验室中的氢氧化钠有没有变质呢?该小组同学对实验室中一瓶氢氧化钠固体样品的成分进行了探究。
【查阅资料】Ⅰ.NaOH在空气中不会转化成NaHCO3。
Ⅱ.BaCl2溶液呈中性,Ba(OH)2是可溶性碱。
Ⅲ.CO2在饱和的NaHCO3溶液中几乎不溶解。
【提出猜想】猜想①:样品中只有NaOH
猜想②:样品中只有Na2CO3
猜想③:样品中既有NaOH又有Na2CO3
NaOH变质反应的化学方程式为______________________。
【实验探究】兴趣小组同学设计如下实验进行探究。
实验操作 | 实验现象与结论 |
1.取少量样品,加足量水。 | 样品全部溶解,得无色溶液。 |
2.取少量实验1所得无色溶液于试管中,滴加足量稀盐酸。 | 有气泡产生,则猜想_____(填“①”、“②”或“③”)不成立。 |
3.取少量实验1所得无色溶液于试管中,滴加 ________溶液。 | 有白色沉淀产生,有关化学方程式为________。 |
4.静置一段时间后,取实验3中试管中上层清液,滴加 _______。 | 对应现象:____ ,则猜想③成立。 |
【定量研究】上述样品变质的程度如何呢?该兴趣小组同学设计如图装置测定样品中Na2CO3的质量分数。
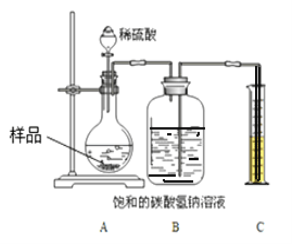
步骤如下:
①按图连接好装置,并检查气密性;
②准确称取该样品1.0g,放入烧瓶内;
③打开分液漏斗活塞,滴加30.0%的稀硫酸至过量,关闭活塞;
④反应结束后,量筒内液体的读数为55.0mL。(已知:室温条件下,CO2的密度为1.6gL﹣1)
⑴ B装置集气瓶内原有的空气对实验结果____(填“有”或“没有”)影响。)
⑵ B中集气瓶盛装的饱和的碳酸氢钠溶液不能用水代替,其理由是___________________;
⑶ 充分反应后,装置A中残留的二氧化碳对实验结果是否有明显影响?____(填“有”或“没有”)
⑷ 计算该样品中Na2CO3的质量分数______(写出计算过程,结果保留到0.1%)。