题目内容
密闭容器中有甲、乙两种物质各10 g,加热一段时间后测得容器中各物质的质量如下表所示
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应后质量/ g | 1.6 | X | 0.9 | 2.2 |
A.该反应为化合反应
B.X="5.3"
C.该反应中甲和乙的质量比为84: 53
D.丙、丁一定是单质
C
解析试题分析:由反应前、后的质量关系可知,反应前甲为10,反应后为1.6g,质量减少了8.4g,是反应物;丙反应前是0g,反应后为0.9g,质量增加了0.9g,是生成物;丁反应前为0g,反应后为2.2g,质量增加了2.2g,是生成物;根据质量守恒定律可知,乙是生成物,生成了5.3g,即x是10+5.3=15.3g。该反应可表示为甲→乙+丙+丁,是分解反应,丙、丁可能是单质;该反应中甲和乙的质量比为8.4:5.3="84:53" ;故选C。
考点:质量守恒定律及其应用

练习册系列答案
相关题目
化学方程式书写正确的是
A.2KClO3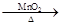 2KCl+3O2 2KCl+3O2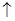 |
B.4P+5O2 2P2O5↓ 2P2O5↓ |
C.CaO+H2O CaO2H2 CaO2H2 |
D.Cu+O2 CuO CuO |
“物质的量”是国际单位制中的一个基本物理量,有关说法正确的是
| A.2克H2中含有1mol氢 |
| B.1mol氧气的摩尔质量为32g |
| C.1mol任何物质都约含有6.02×1023个分子 |
| D.质量相等的O2和O3,它们的物质的量之比为3:2 |
图1是元素周期表中铝元素的部分信息,图2是铝原子的结构示意图。下列说法不正确的是
| A.铝元素原子核内的质子数为13 |
| B.铝的相对原子质量为26.98 g |
| C.铝原子的核外电子分三层排布 |
| D.铝元素的化学性质与铝原子的最外层电子数有密切的关系 |
决定元素种类的是
| A.质子数 | B.中子数 | C.电子数 | D.最外层电子数 |
下列化学方程式不正确的是
A.细铁丝在氧气中燃烧:3Fe +2O2 Fe3O4 Fe3O4 |
| B.铁丝与硫酸铜溶液反应:Fe+CuSO4=Cu+FeSO4 |
C.碳不完全燃烧:2C+O2 2CO 2CO |
D.用赤铁矿石(主要成分:Fe2O3)炼铁:CO+Fe2O3 2Fe+CO2 2Fe+CO2 |
某药剂瓶上标识:每片含钙600毫克。这里的“钙”是指
| A.原子 | B.分子 | C.元素 | D.单质 |
在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:试判断该密闭容器中发生的反应属于( )
| 物质 | X | Y | Z | Q |
| 反应前质量/g | 2 | 2 | 78 | 5 |
| 反应后质量/g | 待测 | 24 | 0 | 14 |
A.分解反应 B.置换反应 C.化合反应 D.复分解反应
C3N4是一种新型材料,它的硬度比金刚石还高,可做切割工具,在C3N4中,C的化合价为+4,则N的化合价是
| A.+5 | B.+3 | C.+1 | D.﹣3 |