题目内容
【题目】某化学兴趣小组准备开展二氧化碳的实验室制取与性质实验活动,实验中需制备约1.1 g二氧化碳气体。为此,实验室李老师准备了足量大理石和稀盐酸.以及相关的仪器、药品.请回答:
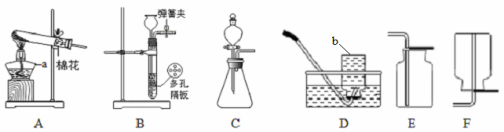
(1)实验室里制取二氧化碳的发生装置与______________相似(填序号)
A.用高锰酸钾制氧气 B.用过氧化氢溶液制氧气
(2)计算实验室准备的大理石中至少含有碳酸钙的质量(杂质不参加反应)
【答案】(1)B(2)2.5g
【解析】
试题分析:(1)根据反应物的状态和反应条件选择发生装置,实验室用石灰石和稀盐酸制取二氧化碳,属固液在常温下的反应,故选B;
(2)利用化学方程式,根据反应的质量比即可计算出碳酸钙的质量。
解:设大理石中至少含有CaCO3的质量为x。
CaCO3 + 2HCl = CaCl2 + CO2↑ + H2O
100 44
x 1.1 g
![]() =
= ![]()
x = 2.5 g
答:大理石中至少含有CaCO3的质量为2.5 g。

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目